Hòa tan hết 3,6 gam một lượng bột kim loại R hóa trị không đổi vào dung dịch hydrochloric acid thu được 4,958 dm3 khí (đkc) và dung dịch chứa t gam muối. Tìm kim loại R và tính t (2 cách)?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi hóa trị của R là n và số mol Sn và R lần lượt là a và b mol
+/ Khi phản ứng với HCl :
Sn + HCl → SnCl2 + H2
R + nHCl → RCln + 0,5nH2
+/ Khi đốt trong oxi :
Sn + O2 → SnO2
2R + 0,5nO2 → R2On
=> Ta có : nH2 = a + 0,5nb = 0,225 mol
Và nO2 = a + 0,25nb = 0,165 mol
=> a = 0,105 mol ; nb = 0,24 mol
Có mmuối = 0,105.190 + 0,24/n . (R + 35,5n) = 36,27
=>R = 32,5n
=>Cặp n =2 ; R =65 (Zn) thỏa mãn
=>B

a)
Gọi số mol R là a (mol)
PTHH: 2R + nH2SO4 --> R2(SO4)n + nH2
a------------------------->0,5an
mtăng = mR - mH2 = a.MR - 2.0,5an = a.MR - an = 1,2 (1)
PTHH: 4R + nO2 --to--> 2R2On
a--------------->0,5a
=> \(0,5a\left(2.M_R+16n\right)=2,55\)
=> a.MR + 8an = 2,55 (2)
(1)(2) => a.MR = 1,35; an = 0,15
=> \(M_R=9n\left(g/mol\right)\)
Xét n = 3 thỏa mãn => MR = 27 (g/mol)
=> R là Al
a = 0,05 (mol)
m = 1,35 (g)
b)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
=> VO2 = 0,0375.22,4 = 0,84 (l)
=> Vkk = 0,84 : 20% = 4,2 (l)

2 khí không màu, không hóa nâu trong không khí và là sản phẩm khử của N+5 chỉ có thể là N2 và N2O
-TH1: 21,19 gam muối không có muối NH4NO3
Theo bảo toàn nguyên tố M ta có: nM= nM(NO3)2
→ m M m M ( N O 3 ) 2 = M M M M ( N O 3 ) 2 → 7 , 15 21 , 19 = M M + 62 , 2
→M= 63,148 Loại
Do đó trường hợp này loại
-TH2: 21,19 gam muối có muối NH4NO3
QT cho e:
M → M2++ ne (1)
7,15/M 7,15.2/M
QT nhận e : nkhí= 0,02 mol. Mà số mol hai khí bằng nhau nên n N 2 O = n N 2 =0,01mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (2)
0,08 0,1 ← 0,01 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (3)
0,1 0,12← 0,01 mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (4)
8x xmol
Đặt số mol muối NH4+ là x mol
Theo ĐL BT e: ne cho= ne nhận nên 7,15.2/M= 0,08 + 0,1+8x (*1)
Mặt khác : mmuối= mM(NO3)2+ mNH4NO3= 7,15/M. (M+124)+80x= 21,19 (*2)
Từ (*1) và (*2) ta có: x= 5.10-3 và M=65. M là Zn
Đáp án D

Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.

a) Ta có \(m_{muôi}=m_{KL}+m_{Cl^-}\\ \Leftrightarrow m_{Cl^-}=m_{muôi}-m_{KL}=14,25-3,6=10,65g\\ \Rightarrow n_{Cl^-}=\dfrac{10,65}{35,5}=0,3mol\)
Theo bảo toàn nguyên tố Cl: \(n_{HCl}=n_{Cl^-}=0,3mol\)
Theo bảo toàn nguyên tố H: \(n_{H_2}=\dfrac{1}{2}\cdot n_{HCl}=\dfrac{1}{2}\cdot0,3=0,15mol\\ \Rightarrow V=0,15\cdot22,4=3,36l\)
Ta có PTHH: \(M+2HCl\rightarrow MCl_2+H_2\uparrow\)
----------------0,15-------------------------0,15---(mol)
\(\Rightarrow M=\dfrac{3,6}{0,15}=24\)(g/mol) => M là Magie (Mg)
b) \(n_{CuO}=\dfrac{16}{80}=0,2mol\)
Ta có quá trình phản ứng:
\(CuO+H_2\rightarrow Cu+H_2O\)
-0,15---0,15-----0,15----------(mol)
\(\Rightarrow a=m_{CuO\left(dư\right)}+m_{Cu}=\left(16-0,15\cdot80\right)+64\cdot0,15=13,6g\)
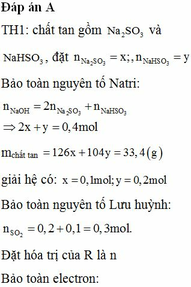

\(n_{H_2}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\)
PTHH: \(2R+2nHCl\rightarrow2RCl_n+nH_2\uparrow\)
\(\dfrac{0,4}{n}\)<-----0,4--------\(\dfrac{0,4}{n}\)<------0,2
\(\rightarrow M_R=\dfrac{3,6}{\dfrac{0,4}{n}}=9n\left(\dfrac{g}{mol}\right)\)
Xét n = 3 TM => MR = 27 => R là Al
Cách 1: \(t=m_{AlCl_3}=\dfrac{0,4}{3}.133,5=17,8\left(g\right)\)
Cách 2: \(n_{Cl}=n_{HCl}=0,4\left(mol\right)\)
BTNT: \(t=m_{Al}+m_{Cl}=3,6+0,4.35,5=17,8\left(g\right)\)