Câu 35: Cho hỗn hợp gồm Na và Al có tỉ lệ số mol tương ứng 1:2 vào nước (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (ở đkc) và m gam chất rắn không tan. Giá trị của m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
n H 2 = 8 , 96 22 , 4 = 0 , 4 mol
Gọi số mol Na là a mol => số mol của Al là 2a mol
m gam chất rắn không tan là Al => Al dư sau phản ứng với NaOH
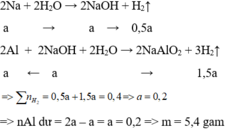

Giải thích:
Gọi số mol của Na và Al lần lượt là x và 2x (mol)
Na + H2O → NaOH + 0,5H2
x x 0,5x
Al + NaOH + H2O → NaAlO2 + 1,5H2
x ← x → x → 1,5x
nH2 = 0,4 => 0,5x + 1,5x = 0,4 => x = 0,2
Chất rắn không tan là Al dư: nAl dư = 2x – x = x = 0,2 mol
=> m = mAl dư = 27.0,2 = 5,4 gam
Đáp án D

Chọn D
Gọi số mol Na là x mol → số mol Al là 2x mol. Theo bài ra chất rắn không tan sau phản ứng là Al dư.


Đáp án : C
Na + H2O -> NaOH + ½ H2
NaOH + Al + H2O -> NaAlO2 + 3/2 H2
=> nH2 = 2nNa => nNa = 0,2 mol = nAl pứ => nAl bđ= 2nNa = 0,4 mol
=> m = mAl không tan = 0,2.27 = 5,4g

Đáp án : A
Na + H2O à NaOH + ½ H2
NaOH + Al + H2O à NaAlO2 + 3/2 H2
Do kim loại dư => nNa = 2nH2 => nNa = 0,2 mol
=> nAl = 2nNa = 0,4 mol
=> nAl dư = nNa – nAl = 0,2 mol
=> m = 5,4g
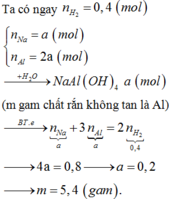

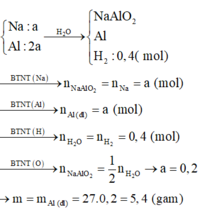
Gọi số mol Na và Al lần lượt là 2x và 4x (mol)
Khi cho hỗn hợp vào nước ta có thứ tự phản ứng:
2Na + 2H2O → 2NaOH + H2
2x ---------------------->2x x
Al + NaOH + H2O → NaAlO2 + 1,5H2
2x 2x 3x
=> ΣnH2 = x + 3x = 8,96:22,4 = 0,4
=> x = 0,1
=> nAl dư = 4x - 2x = 0,2 mol
<=> m CR không tan = mAl dư = 0,2.27 = 5,4 gam