cho 28,8g hỗn hợp gồm đồng và sắt tác dụng với dung dịch axit sunfuric 17% thì thu được 8,96l khí hidro.
a)Tính thành phần % theo khối lượng của mỗi kim loại trong hỗn hợp.
b)Tính khối lượng dung dịch axit sunfuric đã dùng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sửa đề: 6,4 gam hh \(\rightarrow\) 6,45 gam hh
a) Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow24a+27b=6,45\) (1)
Ta có: \(n_{H_2}=\dfrac{7,28}{22,4}=0,325\left(mol\right)\)
Bảo toàn electron: \(2a+3b=0,65\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=n_{Mg}=0,1\left(mol\right)\\b=n_{Al}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1\cdot24}{6,4}\cdot100\%=37,5\%\\\%m_{Mg}=62,5\%\end{matrix}\right.\)
b) Ta thấy với 6,45 gam hh thì có 0,1 mol Mg và 0,15 mol Al
\(\Rightarrow\) Trong 12,9 gam hh thì chứa 0,2 mol Mg và 0,3 mol Al
Gọi \(n_{SO_2}=x\left(mol\right)\)
Bảo toàn electron: \(2\cdot0,2+3\cdot0,3=2x\) \(\Rightarrow x=n_{SO_2}=0,65\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,65\cdot22,4=14,56\left(l\right)\)
gọi số mol của Mg là x mol ; Al là y mol => 24x + 27y =6,4
n khí = 7,28/22,4=0,325 mol
bảo toàn e ta có
Mg + H2SO4 --> MgSO4 + H2
x x mol
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
y 3/2 y mol
=> x + 3/2y=0,325
=> x=11/120 mol ; y=7/45 mol
=> mMg11/120*24=2,2g => %mMg = 2,2*100/6,4=34,375%
=>%mAl=100-34,375=65,625%

PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
\(Cu+2H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}CuSO_4+SO_2\uparrow+2H_2O\)
Ta có: \(n_{SO_2}=\dfrac{0,112}{22,4}=0,005\left(mol\right)=n_{Cu}\)
\(\Rightarrow m_{Cu}=0,005\cdot64=0,32\left(g\right)\) \(\Rightarrow m_{Mg}=10,6-0,32=10,28\left(g\right)\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{HCl}=2n_{H_2}=0,2(mol)\\ a,C_{M_{HCl}}=\dfrac{0,2}{0,1}=2M\\ b,n_{Fe}=n_{H_2}=0,1(mol)\\ \Rightarrow m_{Fe}=0,1.56=5,6(g)\\ \Rightarrow m_{Cu}=20-5,6=14,4(g)\\ c,\%m_{Fe}=\dfrac{5,6}{20}.100\%=28\%\\ \%m_{Cu}=100\%-28\%=72\%\)

2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
x 3/2 x mol
F e + H 2 S O 4 → F e S O 4 + H 2
y y mol
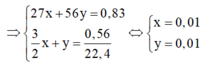
⇒ % m A l = 0,01.27 0,83 .100 = 32,53 % ⇒ % m F e = 100 % − 32,53 % = 67,47 %
⇒ Chọn D.

\(m_{Zn}=60,5-28=32,5g\\
n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\\
n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,5 0,5 0,5
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,5 0,5 0,5
\(V_{H_2}=\left(0,5+0,5\right).22,4=22,4\left(L\right)\\
m_{Mu\text{ối}}=\left(0,5.136\right)+\left(0,5.127\right)=131,5g\)

Đáp án C
Gọi a, b là số mol của Al và Fe trong 8,3 g hỗn hợp ban đầu


a,\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: x x
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}65x+56y=30,7\\x+y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Zn}=\dfrac{0,3.65.100\%}{30,7}=63,52\%;\%m_{Fe}=100\%-63,52\%=36,48\%\)
b,
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,3 0,6
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,4
nHCl = 0,6+0,4 = 1 (mol)
\(V_{ddHCl}=\dfrac{1}{2}=0,5\left(l\right)=500\left(ml\right)\)

a) Gọi số mol CH3COOH, C2H5OH là a, b (mol)
=> 60a + 46b = 25,8 (1)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2Na + 2CH3COOH --> 2CH3COONa + H2
a------------------------->0,5a
2Na + 2C2H5OH --> 2C2H5ONa + H2
b--------------------->0,5b
=> 0,5a + 0,5b = 0,25 (2)
(1)(2) => a = 0,2 (mol); b = 0,3 (mol)
=> \(\left\{{}\begin{matrix}\%m_{CH_3COOH}=\dfrac{0,2.60}{25,8}.100\%=46,51\%\\\%m_{C_2H_5OH}=\dfrac{0,3.46}{25,8}.100\%=53,49\%\end{matrix}\right.\)
b)
\(n_{CH_3COOC_2H_5}=\dfrac{13,2}{88}=0,15\left(mol\right)\)
PTHH: CH3COOH + C2H5OH --H2SO4(đ),to--> CH3COOC2H5 + H2O
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\) => Hiệu suất tính theo CH3COOH
PTHH: CH3COOH + C2H5OH --H2SO4(đ),to--> CH3COOC2H5 + H2O
0,15<---------------------------------0,15
=> \(H=\dfrac{0,15}{0,2}.100\%=75\%\)
a)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
0,4<--0,4<--------------0,4
=> mFe = 0,4.56 = 22,4 (g)
\(\%m_{Fe}=\dfrac{22,4}{28,8}.100\%=77,78\%\Rightarrow\%m_{Cu}=100\%-77,78\%=22,22\%\)
b) \(m_{H_2SO_4}=0,4.98=39,2\left(g\right)\Rightarrow m_{dd.H_2SO_4}=\dfrac{39,2.100}{17}=\dfrac{3920}{17}\left(g\right)\)