nguyên tố A có số hiệu nguyên tử là 17 chu kì 3 và nhóm VII. nêu (clo) cấu tạo và tính chất đặc chưng của nguyên tố A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Nguyên tố X có số hiệu nguyên tử là 17 => đó là Cl
- Nguyên tố X có số hiệu nguyên tử là 17 => điện tích hạt nhân là 17+, có 17 proton, 17 electron
- Nguyên tố X ở chu kì 3 => có 3 lớp electron
- Nguyên tố X thuộc nhóm VII => lớp e ngoài cùng có 7e
Vì X ở cuối chu kì 3 nên X là phi kim mạnh
Đáp án: A

a) Số proton của Clo = số electron = 17
Clo có 3 lớp electron trong nguyên tử và lớp ngoài cùng có 7 .
b)
1. Tác dụng với kim loại
Clo là phi kim mạnh nên khi tác dụng với kim loại nhiều hóa trị thường đẩy kim loại đó lên hóa trị cao nhất .
2. Tác dụng với phi kim
(cần có nhiệt độ hoặc có ánh sáng)
3. Tác dụng với nước và dung dịch kiềm
Cl2 tham gia phản ứng với vai trò vừa là chất ôxi hóa, vừa là chất khử.
a. Tác dụng với nuớc
Khi hoà tan vào nước, một phần Clo tác dụng (Thuận nghịch)
Cl20 + H2O → HCl + HClO (Axit hipoclorơ)
Axit hipoclorơ có tính oxy hoá mạnh, nó phá hửy các màu vì thế nước clo hay clo ẩm có tính tẩy màu do.
b. Tác dụng với dung dịch bazơ
4. Tác dụng với muối của các halogen khác
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2FeCl2 → 2FeCl3
3Cl2 + 6FeSO4 → 2Fe2(SO4)3 + 2FeCl3
Cl2 + 2KI → 2KCl + I2
5. Tác dụng với chất khử khác
6. Phản ứng thế, phản ứng cộng, phản ứng phân huỷ với một số hợp chất hữu cơ

a) A có 8 electron, 8 proton
b) Câu hình e: 1s22s22p4
=> A có 6e lớp ngoài cùng
=> A có tính chất của phi kim
c)
- A là O (oxi)
- Trong chu kì 2, 2 nguyên tố lân cận với O là N, F
Trong 1 chu kì, theo chiều tăng điện tích hạt nhân, tính phi kim tăng dần
=> N < O < F (Xét theo tính phi kim)
- Trong nhóm VIA, nguyên tố lân cận với O là S
Trong 1 nhóm A, theo chiều tăng điện tích hạt nhân, tính phi kim giảm dần
=> O > S (Xét theo tính phi kim)
a: Do A có Z=8 nên A là oxi
Cấu tạo nguyên tử là \(O=O\)
b: Tính chất hóa học đặc trưng là tính phi kim, có tính oxi hóa mạnh

a)A : 1s22s22p63s23p64s2
b) tính chất đó là tính chất của tính khử mạnh , tính bazo
c) yếu hơn K , nhưng mạnh hơn Ga, Ge

số e: 8
ĐTHN: 8+
số lớp e: 2
số e lớp ngoài cùng: 6
trong chu kì 2: N<O<F
trong nhóm VI: O>S
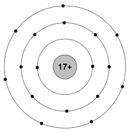
- Nguyên tố X có số hiệu nguyên tử là 17 => đó là Cl
- Nguyên tố X có số hiệu nguyên tử là 17 => điện tích hạt nhân là 17+, có 17 proton, 17 electron
- Nguyên tố X ở chu kì 3 => có 3 lớp electron
- Nguyên tố X thuộc nhóm VII => lớp e ngoài cùng có 7e
Vì X ở cuối chu kì 3 nên X là phi kim mạnh