Đem đốt cháy V lít hỗn hợp khí gồm H2 và O2. Sau phản ứng thu được hỗn hợp chất khí có tỉ khối so với H2 là 14. xác định %V các khí trong hỗn hợp đầy
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giả sử các khí được đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
Gọi số mol CH4, C2H6 là a, b (mol)
=> \(a+b=\dfrac{25}{1}=25\left(mol\right)\) (1)
\(n_{O_2}=\dfrac{95}{1}=95\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a---->2a---------->a
2C2H6 + 7O2 --to--> 4CO2 + 6H2O
b------>3,5b-------->2b
=> \(\left\{{}\begin{matrix}n_{O_2\left(dư\right)}=95-2a-3,5b\left(mol\right)\\n_{CO_2}=a+2b\left(mol\right)\end{matrix}\right.\)
=> \(95-a-1,5b=\dfrac{60}{1}=60\)
=> a + 1,5b = 35 (2)
(1)(2) => a = 5; b = 20
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{5}{25}.100\%=20\%\\\%V_{C_2H_6}=\dfrac{20}{25}.100\%=80\%\end{matrix}\right.\)
\(\overline{M}_A=\dfrac{5.16+20.30}{5+20}=27,2\left(g/mol\right)\)
\(\overline{M}_B=20,5.2=41\left(g/mol\right)\)
=> \(d_{A/B}=\dfrac{27,2}{41}\approx0,663\)

Chọn C.
Đặt CTTQ của X là CxH4 Þ 12x + 4 = 28 Þ x = 2
Khi đốt cháy X thu được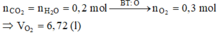

Gọi số mol H2, O2 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{22,4}{22,4}=1\\M_B=\dfrac{2a+32b}{a+b}=5,5.2=11\left(g/mol\right)\end{matrix}\right.\)
=> a = 0,7 (mol); b = 0,3 (mol)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,7}{2}>\dfrac{0,3}{1}\) => H2 dư, O2 hết
PTHH: 2H2 + O2 --to--> 2H2O
0,6<--0,3------->0,6
=> \(\left\{{}\begin{matrix}m_{H_2O}=0,6.18=10,8\left(g\right)\\m_{H_2\left(dư\right)}=\left(0,7-0,6\right).2=0,2\left(g\right)\end{matrix}\right.\)

Đáp án C
Nhận thấy đốt cháy X tương đương đốt cháy metan
→ nCH4 = nO2 : 2 = 0,15 mol
Luôn có mCH4 = mX→ nX =
0
,
15
.
16
4
,
8
.
2
= 0,25 mol
nX - nCH4 = nCH4 pư → nCH4 pứ = 0,1 mol
Vậy H =
0
,
1
0
,
15
×100% = 66,67%.
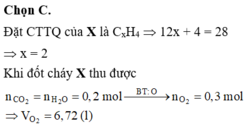

Gọi a (mol) và b (mol) lần lượt là số mol khí H2 và khí O2 ban đầu.
Phân tử khối trung bình của hỗn hợp khí thu được sau phản ứng là 14.2=28 (g/mol), hỗn hợp gồm H2O (a mol) và O2 (b-a/2 mol).
18a+32(b-a/2)=(a+b-a/2).28 \(\Rightarrow\) b=3a.
Thành phần phần trăm các khí trong hỗn hợp ban đầu:
%Vkhí hiđro=\(\dfrac{a}{a+b}\).100%=\(\dfrac{a}{5a}\).100%=20%, suy ra %Vkhí oxi=100%-20%=80%.
Xin lỗi! Mình làm sai rồi.
Chữa:
Gọi a (mol) và b (mol) lần lượt là số mol khí H2 và khí O2 ban đầu.
Phân tử khối trung bình của hỗn hợp khí thu được sau phản ứng là 14.2=28 (g/mol), hỗn hợp gồm H2O (a mol) và O2 (b-a/2 mol).
18a+32(b-a/2)=(a+b-a/2).28 ⇒ b=3a.
Thành phần phần trăm các khí trong hỗn hợp ban đầu:
%Vkhí hiđro=\(\dfrac{a}{a+b}\).100%=\(\dfrac{a}{4a}\).100%=25%, suy ra %Vkhí oxi=100%-25%=75%.