Chia 20,8 gam hỗn hợp gồm hai anđehit đơn chức là đồng đẳng kế tiếp thành hai phần bằng nhau. Phần một tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 đun nóng, thu được 108 gam Ag. Phần hai tác dụng hoàn toàn với H2 dư (xúc tác Ni, t0 ), thu được hỗn hợp X gồm hai ancol (rượu) Y và Z (MY < MZ). Đun nóng X với H2SO4 đặc ở 140oC, thu được 4,52 gam hỗn hợp ba ete. Biết hiệu suất phản ứng tạo ete của Y bằng 50%. Xác định công thức của hai anđehit và tính hiệu suất tạo ete của Z.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp B
Phần 1: n A g = 108 108 = 1 m o l
Trường hợp 1: Hỗn hợp anđehit không chứa HCHO.
n X = 1 2 n A g = 0 , 5 m o l ⇒ M ¯ X = 10 , 4 0 , 5 = 20 , 8 < M H C H O . Loại.
Trường hợp 2: Hỗn hợp anđehit là HCHO (y mol) và CH3CHO (z mol)
⇒ 30 y + 44 z = 10 , 4 g 4 y + 2 z = 1 m o l ⇒ y = 0 , 2 z = 0 , 1
Giả sử hiệu suất tạo ete của Y là H%
Số mol H2O tạo thành 1 2 n a n c o l = 0 , 2 H % + 0 , 1.0 , 5 2 = 0 , 1 H % + 0 , 025
Áp dụng định luật bảo toàn khối lượng có:
32.0,2H% + 46.0,1.0,5 = 4,52 +18.(0,1H% + 0,025)
⇒ H% = 58,04%

Đáp án : A
Nếu trong hỗn hợp không có H-CHO thì số mol trong phần 1 là 0,5 mol nên tổng là 1 mol => M trung bình = 20,8 => Loại
Vậy 2 andehit là HCHO (x mol) và CH3-CHO (y mol) (số mol trong hỗn hợp ban đầu)
Lập hệ ta có: 30x + 44y = 20,8 ; (4x + 2y)/2 = 1;
=> x = 0,4 ; y = 0,2
Vậy phần 2 có 0,2 mol HCHO ; 0,1 mol CH3CHO tạo ra 0,1 mol CH3OH và phản ứng 0,1 mol ; 0,1 mol CH3CH2OH và phản ứng x mol.
Số mol H2O = 1/2 tổng số mol ancol.
Bảo toàn khối lượng ta có: 32.0,l + 46.x – 18.(0,1 + x)/2 = 4,52 => x = 0,06
H = 0,06/0,1 = 60%

Đáp án B
► Xét 1 phần ⇒ mhỗn hợp anđehit = 20,8 ÷ 2 = 10,4(g).
GIẢ SỬ không chứa HCHO ⇒ nhỗn hợp = nAg ÷ 2 = 0,5 mol.
⇒ Mtrung bình hỗn hợp = 10,4 ÷ 0,5 = 20,8 ⇒ loại
⇒ hỗn hợp gồm HCHO và CH3CHO với số mol là 0,2 và 0,1.
► X gồm 0,2 mol CH3OH (Y) và 0,1 mol C2H5OH (Z).
Đặt hiệu suất tạo ete của Z = x ⇒ nZ phản ứng = 0,1x mol.
nY phản ứng = 0,2 × 0,5 = 0,1 mol 2 ancol → 1 ete + 1H2O.
⇒ nH2O = nancol phản ứng ÷ 2 = (0,05 + 0,05x) mol.
Bảo toàn khối lượng: 32.0,1 + 46.0,1x = 4,52 + 18.(0,05 + 0,05x)
⇒ x = 0,6 = 60%

Đáp án B
► Xét 1 phần ⇒ mhỗn hợp anđehit = 20,8 ÷ 2 = 10,4(g).
GIẢ SỬ không chứa HCHO ⇒ nhỗn hợp = nAg ÷ 2 = 0,5 mol.
⇒ Mtrung bình hỗn hợp = 10,4 ÷ 0,5 = 20,8 ⇒ loại
⇒ hỗn hợp gồm HCHO và CH3CHO với số mol là 0,2 và 0,1.
► X gồm 0,2 mol CH3OH (Y) và 0,1 mol C2H5OH (Z).
Đặt hiệu suất tạo ete của Z = x ⇒ nZ phản ứng = 0,1x mol.
nY phản ứng = 0,2 × 0,5 = 0,1 mol || 2 ancol → 1 ete + 1H2O.
||⇒ nH2O = nancol phản ứng ÷ 2 = (0,05 + 0,05x) mol.
Bảo toàn khối lượng: 32.0,1 + 46.0,1x = 4,52 + 18.(0,05 + 0,05x)
||⇒ x = 0,6 = 60%

Chọn đáp án B.
Phần 1: 10,4 gam hỗn hợp + AgNO3 / NH3 thu được 1 mol Ag.
Nhận xét: 10,4:0,5 = 20,8 → hai anđehit phải có HCHO → anđehit còn lại là CH3CHO.
4x + 2y = 1
30x + 44y = 10,4
→x =0,2; y = 0,1→ có 0,2 mol HCHO và 0,1 mol CH3CHO.
Từ kết quả phần 1 → hỗn hợp X gồm 0,2 mol CH3OH (Y) và 0,1 mol CH3CH2OH (Z).
Phản ứng ete hóa: 2 ancol → 1 ete + 1H2O
Gọi hiệu suất phản ứng tạo ete của Z là h.
→ Lượng ancol phản ứng: 0,1 mol CH3OH và 0,1h mol C2H5OH → số mol H2O là (0,05 + 0,05h).
BTKL có: mancol = meste + mH2O → 0,1 x 32 + 0,1h x 46 = 4,52 +(0,05 + 0,05h) x18 → h = 0,6

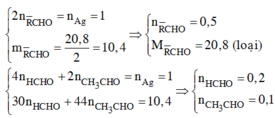
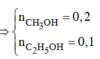
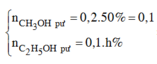
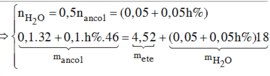




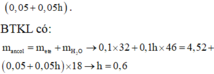
\(n_{Ag}=\dfrac{108}{108}=1\left(mol\right)\)
\(m_{andehit\left(trong.mỗi.phần\right)}=\dfrac{20,8}{2}=10,4\left(g\right)\)
- Nếu trong hỗn hợp không có HCHO
Gọi công thức chung của 2 andehit là RCHO
RCHO --> 2Ag
0,5<-----1
=> \(M_{RCHO}=\dfrac{10,4}{0,5}=20,8\left(g/mol\right)\)
=> Loại
=> Trong hỗn hợp ban đầu có HCHO
=> Andehit còn lại là CH3CHO
Gọi số mol HCHO, CH3CHO trong mỗi phần là a, b (mol)
=> 30a + 44b = 10,4 (1)
HCHO --> 4Ag
a------>4a
CH3CHO --> 2Ag
b------->2b
=> 4a + 2b = 1 (2)
(1)(2) => a = 0,2 (mol); b = 0,1 (mol)
- Phần 2:
X \(\left\{{}\begin{matrix}CH_3OH:0,2\left(mol\right)\\C_2H_5OH:0,1\left(mol\right)\end{matrix}\right.\)
\(n_{CH_3OH\left(pư\right)}=\dfrac{0,2.50}{100}=0,1\left(mol\right)\)
Giả sử hiệu suất tạo ete của C2H5OH là a%
=> \(n_{C_2H_5OH\left(pư\right)}=\dfrac{0,1a}{100}=0,001a\left(mol\right)\)
\(n_{H_2O}=\dfrac{n_{ancol\left(pư\right)}}{2}=\dfrac{0,1+0,001a}{2}\left(mol\right)\)
Theo ĐLBTKL: \(m_{ancol\left(pư\right)}=m_{ete}+m_{H_2O}\)
=> 0,1.32 + 46.0,001a = 4,52 + \(18.\dfrac{0,1+0,001a}{2}\)
=> a = 60