Cho 13 gam một kim loại X ( hóa trị II) tác dụng vừa đủ với 2,24 lít khí Oxi ở đktc, tạo ra oxit bazo. Tìm kim loại đã phản ứng và tính khối lượng oxit thu được.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH : \(2X+O_2\underrightarrow{t^o}2XO\)
0,3 0,15 /mol
Ta có : \(0,3=\dfrac{19,2}{X}\Rightarrow X=64\) => X là Cu
\(m_{CuO}=80.0,3=24\left(g\right)\)
Gọi R là kim loại cần tìm.
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(2R+O_2\underrightarrow{t^o}2RO\)
\(\dfrac{19,2}{R}\) 0,15
\(\Rightarrow\dfrac{19,2}{R}=0,15\cdot2\Rightarrow R=64\Rightarrow Cu\)
Khối lượng oxit: \(m_{CuO}=0,3\cdot80=24g\)

Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
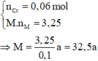
=> a = 2, M = 65 (M là Zn).

Câu 8:
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,2}{1}\), ta được O2 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{H_2}=0,05\left(mol\right)\\n_{H_2O}=n_{H_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,15\left(mol\right)\)
\(\Rightarrow V_{O_2\left(dư\right)}=0,15.22,4=3,36\left(l\right)\)
\(m_{H_2O}=0,1.18=1,8\left(g\right)\)
Bạn tham khảo nhé!
Câu 9:
a, PT: \(2R+O_2\underrightarrow{t^o}2RO\)
Theo ĐLBT KL, có: mR + mO2 = mRO
⇒ mO2 = 4,8 (g)
\(\Rightarrow n_{O_2}=\dfrac{4,8}{32}=0,15\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)
b, Theo PT: \(n_R=2n_{O_2}=0,3\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{19,2}{0,3}=64\left(g/mol\right)\)
Vậy: M là đồng (Cu).
Câu 10:
Ta có: mBaCl2 = 200.15% = 30 (g)
a, m dd = 200 + 100 = 300 (g)
\(\Rightarrow C\%_{BaCl_2}=\dfrac{30}{300}.100\%=10\%\)
⇒ Nồng độ dung dịch giảm 5%
b, Ta có: \(C\%_{BaCl_2}=\dfrac{30}{150}.100\%=20\%\)
⇒ Nồng độ dung dịch tăng 5%.
Bạn tham khảo nhé!

2Al+3H2SO4->Al2(SO4)3+3H2
0,2-----------------------------------0,3
n Al=0,2 mol
=>VH2=0,3.22,4=6,72l
b)
XO+H2-to>X+H2O
0,3-------------0,3
=>0,3=\(\dfrac{19,5}{X}\)
=>X là Zn( kẽm)
a.\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_X=\dfrac{19,5}{M_X}\)
\(XO+H_2\rightarrow\left(t^o\right)X+H_2O\)
\(\dfrac{19,5}{M_X}\) \(\dfrac{19,5}{M_X}\) ( mol )
Ta có:
\(\dfrac{19,5}{M_X}=0,3\)
\(\Leftrightarrow M_X=65\)
=> X là kẽm (Zn)

2K + O2 → 2K2O
nK2O = \(\dfrac{18,8}{94}\)= 0,2 mol => nKphản ứng = 0,2 mol , nO2phản ứng = 0,1 mol
VO2 = 0,1.22,4 = 2,24 lít . Oxi chiếm 1/5 thể tích không khí => V không khí = 2,24.5 = 11,2 lít
mK = 0,2.39 = 7,8 gam
2K + O2 → 2K2O
Nếu có 3,36 lít Oxi phản ứng với 0,2 mol kali => nO2 = \(\dfrac{3,36}{22,4}\)= 0,15mol
Ta có tỉ lệ \(\dfrac{0,2}{2}< \dfrac{0,15}{1}\)=> Oxi dư , kali hết .
Khối lượng sp thu được vẫn tính theo kali => nK2O = 0,2 mol
<=> mK2O = 0,2.94 = 18,8 gam

\(n_{O_2}=\dfrac{1.68}{22.4}=0.075\left(mol\right)\)
\(4R+nO_2\underrightarrow{^{^{t^0}}}2R_2O_n\)
\(\dfrac{0.3}{n}....0.075\)
\(M_R=\dfrac{9.6}{\dfrac{0.3}{n}}=32n\)
Với : \(n=2\Rightarrow R=64\)
\(R:Cu\)
\(CuO:\) Đồng (II) oxit
nO2 = 0,075(mol)
PT
2R + O2 -> (đknd) 2RO
0,15 <- 0,075 (mol)
=> MR = m/n = 9,6 / 0,15 = 64 => R là Cu và oxit là CuO

\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\); \(n_{A\left(OH\right)_2}=\dfrac{34,2}{M_A+34}\left(mol\right)\)
\(A+2H_2O\rightarrow A\left(OH\right)_2+H_2\)
\(\dfrac{34,2}{M_A+34}\) --> \(\dfrac{34,2}{M_A+34}\) ( mol )
\(\rightarrow n_{H_2}=\dfrac{34,2}{M_A+34}=0,2\left(mol\right)\)
\(\Leftrightarrow34,2=0,2M_A+6,8\)
\(\Leftrightarrow0,2M_A=27,4\)
\(\Leftrightarrow M_A=137\) ( g/mol )
--> A là Bari ( Ba )
\(A+H_2O\rightarrow A\left(OH\right)_2+H_2\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ TheoPT:n_{H_2}=n_{A\left(OH\right)_2}=0,2\left(mol\right)\\ \Rightarrow M_{A\left(OH\right)_2}=A+17.2=\dfrac{34,2}{0,2}=171\\ \Rightarrow A=137\left(Ba\right)\)

nO2 = 2,24/22,4 = 0,1 (mol)
PTHH: 2R + O2 -> (t°) 2RO
nRO = 0,1 . 2 = 0,2 (mol)
M(RO) = 16,2/0,2 = 81 (g/mol)
<=> R + 16 = 81
<=> R = 65
<=> R là Zn
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{2,24}{22,4}=0,1mol\)
\(m_{O_2}=n_{O_2}.M_{O_2}=0,1.32=3,2g\)
Vì R hóa trị II nên PTHH là:
\(2R+O_2\rightarrow\left(t^o\right)2RO\)
2 1 2 ( mol )
0,2 0,1
Áp dụng định luật bảo toàn khối lượng, ta có:
\(m_R=16,2-3,2=13g\)
\(M_R=\dfrac{m_R}{n_R}=\dfrac{13}{0,2}=65\) g/mol
\(\Rightarrow R\) là kẽm (Zn)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(2X+O_2\underrightarrow{t^o}2XO\)
\(\dfrac{13}{X}\) 0,1
\(\Rightarrow\dfrac{13}{X}=0,1\cdot2\Rightarrow X=65\)
Vậy X là kẽm Zn.
\(m_{ZnO}=0,2\cdot81=1,62g\)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2R + O2 --to--> 2RO
0,2 0,.1
=> \(M_R=\dfrac{13}{0,2}=65\left(\dfrac{g}{mol}\right)\)
=> R: Zn