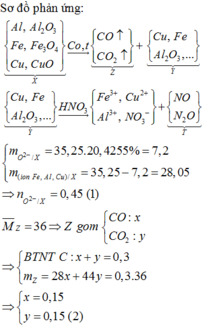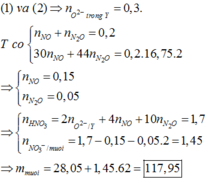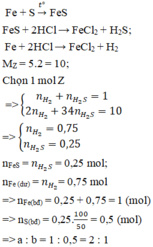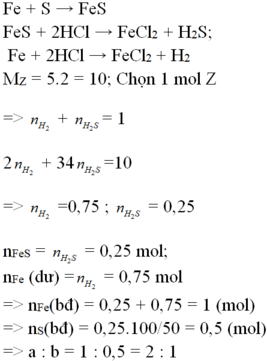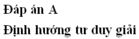Hỗn hợp X gồm Al và S. Nung nóng 10,2g X để phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Hòa tan hoàn Y bằng dung dịch HCl dư thu được hỗn hợp khí Z có tỉ khối so với H2 là 9. Tính %Al về khối lượng ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: \(2Al+3S\underrightarrow{^{t^o}}Al_2S_3\)
Gọi số mol Al là x; S là y.
Ta có phương trình : \(27x+32y=10,2\left(g\right)\)
Vì cho Y tác dụng với HCl thu được hỗn hợp khí nên Al dư
\(\Rightarrow n_{Al_2S_3}=\dfrac{1}{3}n_S=\dfrac{y}{3}\left(mol\right)\)
\(\Rightarrow n_{Al\left(dư\right)}=x-\dfrac{2y}{3}\left(mol\right)\)
PTHH:
\(Al_2S_3+6HCl\rightarrow2AlCl_3+3H_2S\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow n_{H2S}=3n_{Al2S3}=y\left(mol\right);n_{H2}=\dfrac{3}{2}n_{Al}=1,5x-y\left(mol\right)\)
\(M_Z=18\)
Áp dụng quy tắc đường chéo :
\(\Rightarrow\dfrac{n_{H2S}}{n_{H2}}=\dfrac{16}{16}\Rightarrow1,5x-y=y\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
\(\Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{5,4}{10,2}=52,94\%\\\%m_S=100\%-52,94\%=47,06\%\end{matrix}\right.\)

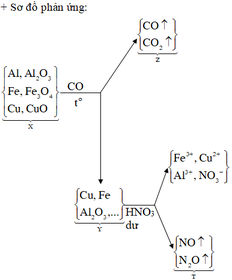
Đ á p á n B S ơ đ ồ p h ả n ứ n g : A l , A l 2 O 3 F e , F e 3 O 4 C u , C u O → C O , t o C O C O 2 C u , F e A l 2 O 3 C u , F e A l 2 O 3 → H N O 3 d ư F e 3 + , C u 2 + A l 3 + , N O 3 - N O N 2 O m O 2 - / X = 35 , 25 . 20 , 4255 % = 7 , 2 m i o n F e , A l , C u / X = 35 , 25 - 7 , 2 = 28 , 05 m O 2 - / X = 0 , 45 1 M Z = 36 ⇒ Z g ồ m C O : x C O 2 : y ⇒ B T N T C : x + y = 0 , 3 m Z = 28 x + 44 y = 0 , 3 . 36 ⇒ x = 0 , 15 y = 0 , 15 2 1 v à o 2 ⇒ m O 2 - / Y = 0 , 45 - 0 , 15 = 0 , 3 n N O + n N 2 O = 0 , 2 30 n N O + 44 n N 2 O = 0 , 2 . 16 , 75 . 2 ⇒ n N O = 0 , 15 n N 2 O = 0 , 05 n H N O 3 = 2 n O 2 - / Y + 4 n N O + 10 n N 2 O = 1 , 7 n N O 3 - ( M u ố i ) = 1 , 7 - 0 , 15 - 0 , 05 . 2 = 1 , 45 ⇒ m M u ố i = 28 , 05 + 1 , 45 . 62 = 117 , 95

Đáp án B
Trong, đặt ![]()
![]()
![]()
=> giải hệ có x = y = 0,15 mol
![]()
![]()
![]()
![]()
![]()
![]()
![]() giải hệ có: a = 0,15 mol; b = 0,05 mol
giải hệ có: a = 0,15 mol; b = 0,05 mol
![]()
![]()
= 0,45 mol
![]()

Phản ứng xảy ra:
\(2Al+3S\underrightarrow{^{t^o}}Al_2S_3\)
Gọi \(\left\{{}\begin{matrix}n_{Al}:x\left(mol\right)\\n_S:y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow27x+32y=10,2\left(g\right)\)
Vì cho Y tác dụng với HCl thu được hỗn hợp khí nên Al dư
\(\Rightarrow n_{Al2S3}=\frac{1}{3}n_S=\frac{y}{3}\left(mol\right)\)
\(\Rightarrow n_{Al\left(dư\right)}=x-\frac{2y}{3}\left(mol\right)\)
\(Al_2S_3+6HCl\rightarrow2AlCl_3+3H_2S\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow n_{H2S}=3n_{Al2S3}=y\left(mol\right);n_{H2}=\frac{3}{2}n_{Al}=1,5x-y\left(mol\right)\)
Ta có:
\(M_Z=9.2=18\)
Áp dụng quy tắc đường chéo:
\(\Rightarrow\frac{n_{H2S}}{n_{H2}}=\frac{y}{1,5x-y}=\frac{16}{16}\Rightarrow1,5x-y=y\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
\(\Rightarrow m=0,2.27=5,4\left(g\right)\Rightarrow\%m_{Al}=\frac{5,4}{10,2}.100\%=52,94\%\)