Tính thể tích oxi cần lấy ở điều kiện tiêu chuẩn để có số phân tử bằng số phân tử trong 88 gam CO2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Số mol CO2 là :
\(\frac{1,5.10^{23}}{6.10^{23}}=0,25mol\)
VCO2 ở đktc : V = 0,25 . 22,4 = 5,6 (lít)

\(N_{Fe_2\left(SO_4\right)_3}=\dfrac{80}{400}.6.10^{23}=1,2.10^{23}\left(PT\right)\\ V_{CO_2}=\dfrac{80}{400}.22,4=4,48L\)
\(n_{Fe_2\left(SO_4\right)_3}=\dfrac{80}{400}=0,2\left(mol\right)\)
\(\Rightarrow N_{Fe_2\left(SO_4\right)_3}=6.10^{23}\cdot0,2=1,2.10^{23}\left(pt\right)\)
Ta có:\(N_{CO_2}=N_{Fe_2\left(SO_4\right)_3}=1,2.10^{23}\)
\(\Rightarrow n_{CO_2}=0,2\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,2.22,4=4,48\left(l\right)\)

CHÚC BẠN HỌC TỐT![]()
Vì SPT bằng nhau \(\Rightarrow\) số mol bằng nhau\(\Rightarrow\) thể tích bằng nhau
Vậy phải lấy 0,56 (l) CO2 để có phân tử đúng bằng số phân tử có trong 560 cm3 khí nitơ (đktc)
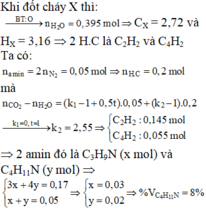
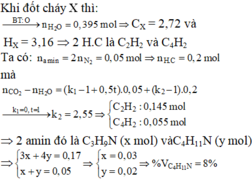
\(n_{CO_2}=\dfrac{88}{44}=2\left(mol\right)\)
\(\text{Số phân tử }CO_2\text{là: }\) \(2\cdot6\cdot10^{23}=12\cdot10^{23}\left(pt\right)\)
\(n_{O_2}=\dfrac{12\cdot10^{23}}{6\cdot10^{23}}=2\left(mol\right)\)
\(V_{O_2}=2\cdot22.4=44.8\left(l\right)\)