15. Phân hủy hoàn toàn 36.75 gam kali clorat KCLO3 ở nhiệt độ cao, sao phản ứng thu đc chất rắn là V lít khí oxi (đktc) a/viết PTHH của phản ứng xảy ra b/ Tính giá trị V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)PTHH:2KClO\(_3\)➞\(^{t^o}\)2KCl+3O\(_2\)
b) n\(_{KClO_3}\)=\(\dfrac{m_{KClO_3}}{M_{KClO_3}}\)=\(\dfrac{12,15}{122,5}\)\(\approx\)0,1(m)
PTHH : 2KClO\(_3\) ➞\(^{t^o}\) 2KCl + 3O\(_2\)
tỉ lệ : 2 2 3
số mol : 0,1 0,1 0,15
V\(_{O_2}\)=n\(_{O_2}\).22,4=0,15.22,4=3,36(l)
c)PTHH : 2Zn + O\(_2\) -> 2ZnO
tỉ lệ : 2 1 2
số mol :0,3 0,15 0,3
m\(_{Zn}\)=n\(_{Zn}\).M\(_{Zn}\)=0,3.65=19,5(g)

\(2KClO_3\rightarrow3O_2+2KCl\)
\(m_{KClO_3}=m_{O_2}+m_{KCl}\)
\(\Rightarrow m_{KCl}=m_{KClO_3}-m_{KCl}=24,5-9,6=14,9\left(g\right)\)

a)\(n_{CuO}=\dfrac{16}{80}=0,2mol\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
b)\(n_{Na}=\dfrac{4,6}{23}=0,2mol\)
\(n_{H_2O}=\dfrac{100}{18}=\dfrac{50}{9}mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(0,2\) \(\dfrac{50}{9}\) 0 0
\(0,2\) 0,2 0,2 0,1
0 \(5,35\) 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)

a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,2 0,1 ( mol )
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{O_2}=0,1.60\%=0,06mol\)
\(2R+\dfrac{1}{2}nO_2\rightarrow\left(t^o\right)R_2O_n\)
\(\dfrac{2,16}{M_R}\) \(\dfrac{2,16n}{M_R}\) ( mol )
\(\Rightarrow\dfrac{2,16n}{M_R}=0,06\)
\(\Rightarrow0,06M_R=2,16n\)
\(\Rightarrow M_R=36n\)
Biện luận:
-n=1 => Loại
-n=2 => Loại
-n=3 => \(M_R=108\) ( g/mol ) R là Bạc ( Ag )
Vậy R là Bạc (Ag)

\(n_{Zn}=\dfrac{36}{65}=0,4\left(mol\right)\)
Pt : \(2Zn+O_2\rightarrow\left(t_o\right)2ZnO|\)
2 1 2
0,4 0,2 0,4
a) \(n_{H2}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
b) \(n_{ZnO}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{ZnO}=0,4.81=32,4\left(g\right)\)
Chúc bạn học tốt
PTHH:\(Zn+\dfrac{1}{2}O_2\xrightarrow[]{t^o}ZnO\)
Ta có: \(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{O_2}=0,2\left(mol\right)\\n_{ZnO}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=0,2\cdot22,4=4,48\left(l\right)\\m_{ZnO}=0,4\cdot81=32,4\left(g\right)\end{matrix}\right.\)

\(a,2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ n_{KMnO_4}=\dfrac{395}{158}=2,5(mol)\\ \Rightarrow n_{O_2}=1,25(mol)\\ \Rightarrow V_{O_2}=1,25.22,4=28(l)\\ \Rightarrow V_{O_2(tt)}=28.85\%=23,8(l)\)
\(b,n_{O_2}=\dfrac{67,2}{22,4}=3(mol)\\ 2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ \Rightarrow n_{KMnO_4}=6(mol)\\ \Rightarrow m_{KMnO_4}=6.158=948(g)\\ \Rightarrow m_{KMnO_4(tt)}=\dfrac{948}{80\%}=1185(g)\)

a. PTHH: \(KMnO_4\rightarrow^{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
b. \(H=100\%\)
\(n_{KMnO_4}=\frac{3,6}{158}=0,023mol\)
Theo phương trình \(n_{O_2}=0,5n_{KMnO_4}=0,046mol\)
\(\rightarrow V_{O_2}=0,0115.22,4.100\%=0,2576l\)
c. H = 80%
\(\rightarrow V_{O_2}=0,0115.22,4.80\%=0,20608l\)
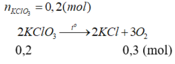
a) 2KClO3 --to--> 2KCl + 3O2
b) \(n_{KClO_3}=\dfrac{36,75}{122,5}=0,3\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,3----------------->0,45
=> V = 0,45.22,4 = 10,08 (l)
nKClO3 = 36,75 : 122,5 = 0,3 (mol)
pthh : 2KClO3 -t--> 2KCl + 3O2
0,3----------------------->0,45 (mol)
=> V= VO2 = 0,45 . 22,4 = 10,08 (L)