Người thợ xây dùng 29,4 kg vôi sống (CaO) hòa vào nước, thu được chất vôi tôi (Ca(OH)2) dùng để quét tường gạch. Hãy tính lượng vôi tôi thu được, biết rằng trong vôi sống có chứa 5% tạp chất không tan.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phần trăm khối lượng vôi sống nguyên chất là:
100%-10%=90%
Khối lượng \(CaO\) nguyên chất:
\(m_{CaO}=\dfrac{210\cdot90\%}{100\%}=189kg\Rightarrow n_{CaO}=3,375mol\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
56 74 kg (theo khối lượng)
189kg x(kg)
\(\Rightarrow56\cdot x=189\cdot74\Rightarrow x=249,75kg\)
Vậy khối lượng thu được là \(m=249,75\cdot80\%=199,8kg\)
mCaCO3 = 210.(100% - 10%) = 189 (kg)
=> \(n_{CaCO_3}=\dfrac{189}{100}=1,89\left(kmol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
1,89 1,89
CaO + H2O ---> Ca(OH)2
1,89 1,89
\(\rightarrow m_{Ca\left(OH\right)_2\left(tt\right)}=1,89.80\%.74=11,888\left(g\right)\)

3) Zn+2HCl->ZnCl2+H2
a) \(n_{Zn}=\frac{13}{65}=0,2mol\)
Vì: \(\frac{0,2}{1}< \frac{0,5}{2}\)=> Zn hết, HCl dư.
\(n_{H_2}=n_{Zn}=0,2mol\)
\(V_{H_2}=0,2.22,4=4,48l\)
H=90%=> VH2 thu được là:4,032l
b) HCl dư: 0,5-(0,2.2)=0,1mol
mHCl=0,1.36,5=3,65g

PTHH: CaCO3 -> CaO + CO2
ta có : 8,4 tấn = 84000000g
6,6 tấn =66000000g
áp dụng định luật bảo toàn khối lượng ta có :
=>mCaCO3=84000000+66000000=150000000g
=>mCaCO3(đem nung)=150000000/100*80=120000000g
b) ta có: 5 tấn =50000000g
1,76 tấn =17600000g
áp dụng định luật bảo toàn khối lượng ta có :
mCaO=50000000+17600000=67600000g

Chọn đáp án C.
Ta có phương trình phản ứng:
![]()
m C a C O 3 = 100 . 80 100 = 80 k g
→ n C a C O 3 = 80 100 = 0 , 8 k m o l
⇒ m C a O = 0 , 8 . 56 = 448 k g
mchất rắn = 44 , 8 + 20 = 64 , 8 k g

CaO (vôi sống) + H2O ---> Ca(OH)2 (vôi tôi)
nCaO = nCa(OH)2 = 166,5/74 = 2,25 kmol.
---> mCaO = 56.2,25 = 126 kg.
Vì chứa 15% tạp chất nên khối lượng CaO lúc đầu cần là: 126/0,85 = 148,23 kg.
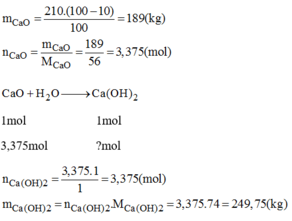

\(m_{CaO}=29.4\cdot\dfrac{95}{100}=27.93\left(g\right)\)
\(n_{CaO}=\dfrac{27.93}{56}=0.49875\left(mol\right)\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(0.49875...........0.49875\)
\(m_{Ca\left(OH\right)_2}=0.49875\cdot74=36.9075\left(g\right)\)