Nung m (gam) hỗn hợp A gồm KMnO4và KClO3 thu được chất rắn B và khí O2. Lúc đó KClO3 phân hủy hoàn toàn, còn KMnO4 phân hủy không hoàn toàn. Trong B có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn O2 thu được ở trên với không khí (Có phần trăm thể tích 20% O2; 80% N2) theo tỷ lệ thể tích tương ứng là 1:3 tạo thành hỗn hợp khí C.Cho toàn bộ khí C vào bình chứa 0,528 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp D...
Đọc tiếp
Nung m (gam) hỗn hợp A gồm KMnO4và KClO3 thu được chất rắn B và khí O2. Lúc đó KClO3 phân hủy hoàn toàn, còn KMnO4 phân hủy không hoàn toàn. Trong B có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn O2 thu được ở trên với không khí (Có phần trăm thể tích 20% O2; 80% N2) theo tỷ lệ thể tích tương ứng là 1:3 tạo thành hỗn hợp khí C.Cho toàn bộ khí C vào bình chứa 0,528 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp D gồm 3 khí (Trong đó O2 chiếm 17,083% về thể tích).
a) Tính phần trăm khối lượng mỗi chất có trong A.
b)Thêm 74,5 gam KCl vào chất rắn B được hỗn hợp E. Cho hỗn hợp E vào dung dịch H2SO4 loãng dư,đun nóng nhẹ cho đến khi phản ứng hoàn toàn. Tính thể tích khí thoát ra (đo đktc).
Câu 8. Đặt 2 cốc A, B có cùng khối lượng lên 2 đĩa cân thăng bằng. Chovào cốc A 102 gam chất rắn AgNO3; cốc B gam chất rắn K2CO3.
a) Thêm 100 gam dung dịch HCl 29,2% vào cốc A; 100 gam dung dịch H2SO4 24,5% vào cốc B cho đến khi phản ứng xảy ra hoàn toàn. Phải thêm bao nhiêu gam nước vào cốc A (hay cốc B) để trở lại thăng bằng?
b) Sau khi cân đã thăng bằng, lấy ½ lượng dung dịch trong cốc A cho vào cốc B. Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc A để cân trở lại thăng bằng?


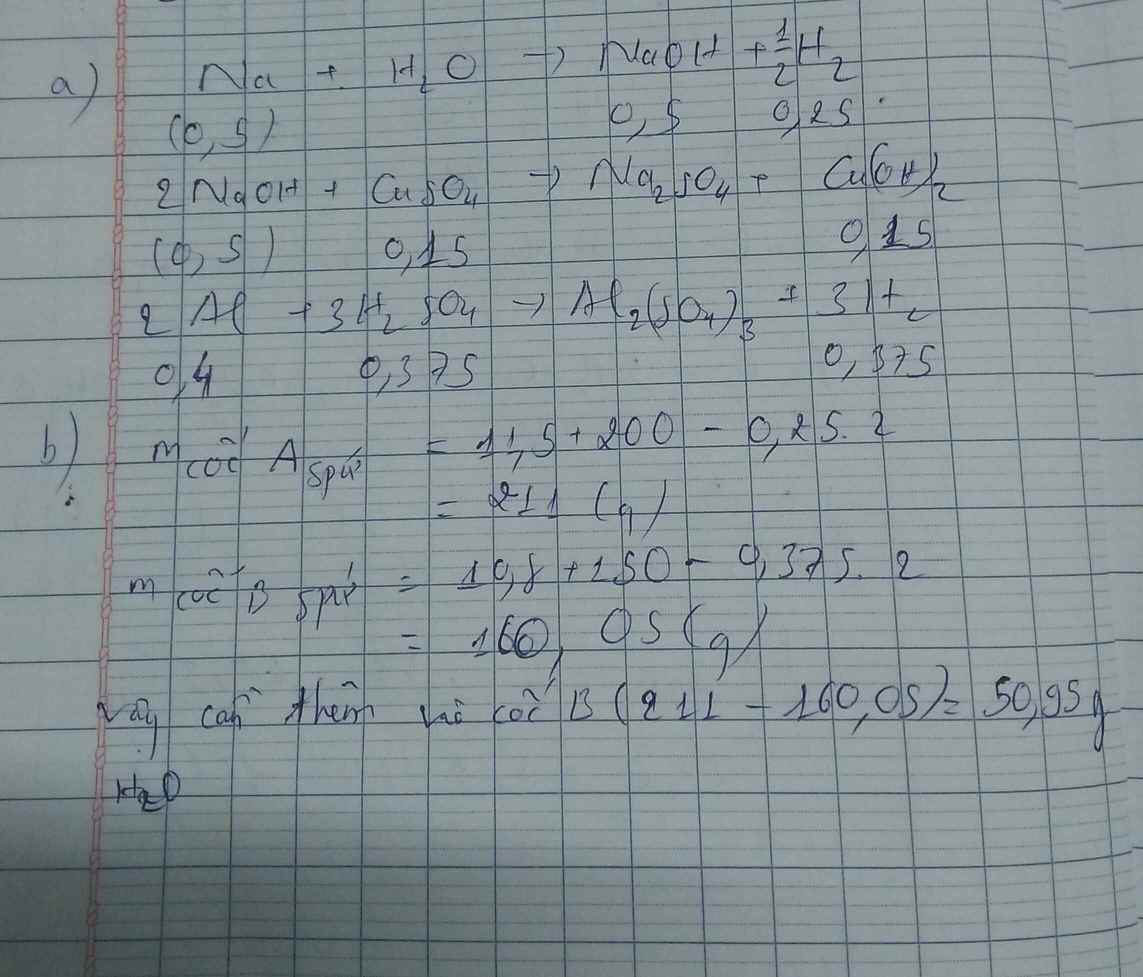
PTHH.
2KClO3 to 2KCl + 3O2 (1)
2KMnO4 to K2MnO4 + MnO2 + O2 (2)
Gọi a là tổng số mol õi tạo ra ở PT(1) và (2), sau khi trộn với không khí ta có trong hỗn hợp X.
nO2= a+ 3a.20%= 1,6a (mol).
nN2= 3a.80% = 2,4a (mol).
Ta có nC= 0,528/12= 0,044 mol
mB= 0,894.100/8,132= 10,994 gam
Theo đề cho trong Y có 3 khí nên xảy ra 2 trươnhg hợp;
Trường hợp 1: Nếu oxi dư, lúc đó các bon cháy theo phản ứng:
C + O2 to CO2 (3)
Tổng số mol khí Y: nY= 0,044.100/22,92= 0,192 mol gồm các khí O2 dư, N2, CO2
Theo PT(3): nO2pư= nC= 0,044 mol
nCO2= nC= 0,044 mol
nO2dư= 1,6- 0,044
nY= 1,6a- 0,044 + 2,4 + 0,044 = 0,192
Giải ra: a= 0,048, mO2 = 0,048.32= 1,536 gam.
Theo đề ta có: mA= mB+ mO2 = 10,944 + 1,536 = 12,53 gam.
Trường hợp 2: Nếu oxi thiếu, lúc đó các bon cháy theo phản ứng:
C + O2 to CO2 (3)
C + O2 to 2CO (4)
Gọi b là số mol CO2 tạo thành, theo PT(3),(4): nCO= 0,044- b
nO2= b+ 0,044-b/2 = 1,6 a
Y gồm N2, CO2, CO và nY= 2,4a + b+ 0,044- b = 2,4 a+ 0,044
%CO2 = b/2,4+ 0,044= 22,92/100
Giải ra: a= 0,204 mol, mO2= 0,204.32= 0,6528 gam
Vậy: mA= mB+ mO2 = 10,944 + 0,6528 = 11,6468 gam gam.