1.Cho 400 ml dung dịch E gồm AlCl3 x mol/lít và Al2(SO4)3 y mol/lít tác dụng với 612 ml dung dịch NaOH 1M, sau khi các phản ứng kết thúc thu được 8,424 gam kết tủa Mặt khác, khi cho 400 ml E tác dụng với dung dịch BaCl2 (dư) thì thu được 33,552 gam kết tủa Tỉ lệ x : y là
2.Cho 200 ml dd gồm MgCl2 0,3M; AlCl3 0,45; HCl 0,55M tác dụng hoàn toàn với V(lít) dd C chứa NaOH 0,02 M và Ba(OH)2 0,01 M Hãy tính thể tich V(lít) cần dùng để thu được kết tủa lớn nhất và lượng kết tủa Al(OH)3 tan hết Tính lượng kết tủa đó (giả sử khi Mg(OH)2 kết tủa hết thì Al(OH)3 tan trong kiềm kh ng đáng kể)
3.Cho 200ml dung dịch NaOH vào 200g dung dịch Al2(SO4)3 1,71% Sau phản ứng thu được 0,78g kết tủa Tính nồng độ mol/l của dung dịch NaOH tham gia phản ứng
giải bằng pthh, không dùng pt ion

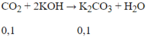
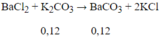

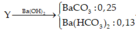
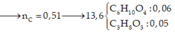

Bài 1:
400ml dd E chứa \(\left\{{}\begin{matrix}AlCl_3:0,4x\left(mol\right)\\Al_2\left(SO_4\right)_3:0,4y\left(mol\right)\end{matrix}\right.\)
Xét TN2:
\(n_{BaSO_4}=\dfrac{33,552}{233}=0,144\left(mol\right)\)
=> \(n_{Al_2\left(SO_4\right)_3}=\dfrac{0,144}{3}=0,048\left(mol\right)\)
=> y = 0,12
Xét TN1:
\(n_{Al\left(OH\right)_3}=\dfrac{8,424}{78}=0,108\left(mol\right)\)
nNaOH = 0,612.1 = 0,612 (mol)
Do \(3.n_{Al\left(OH\right)_3}< n_{NaOH}\) => Kết tủa bị hòa tan 1 phần
PTHH: Al2(SO4)3 + 6NaOH --> 3Na2SO4 + 2Al(OH)3
0,048------>0,288------------------->0,096
AlCl3 + 3NaOH --> 3NaCl + Al(OH)3
0,4x--->1,2x------------------>0,4x
Al(OH)3 + NaOH --> NaAlO2 + 2H2O
(0,324-1,2x)<-(0,324-1,2x)
=> 0,096 + 0,4x - (0,324-1,2x) = 0,108
=> x = 0,21
=> \(\dfrac{x}{y}=\dfrac{0,21}{0,12}=\dfrac{7}{4}\)
Bài 3:
\(n_{Al_2\left(SO_4\right)_3}=\dfrac{200.1,71\%}{342}=0,01\left(mol\right)\)
\(n_{Al\left(OH\right)_3}=\dfrac{0,78}{78}=0,01\left(mol\right)\)
- Nếu kết tủa không bị hòa tan:
PTHH: 6NaOH + Al2(SO4)3 --> 3Na2SO4 + 2Al(OH)3
0,03<-------------------------------0,01
=> \(C_M=\dfrac{0,03}{0,2}=0,15M\)
- Nếu kết tủa bị hòa tan 1 phần
PTHH: 6NaOH + Al2(SO4)3 --> 3Na2SO4 + 2Al(OH)3
0,06<---0,01-------------------------->0,02
Al(OH)3 + NaOH --> NaAlO2 + 2H2O
0,01---->0,01
=> \(C_M=\dfrac{0,06+0,01}{0,2}=0,35M\)
Sao lại báo cáo, chuẩn câu hỏi r còn j