Bài 3: khi đốt cháy sắt trong khí oxi thu được oxit sắt từ Fe3O4. .Tính số gam sắt và thể tích oxi ( đktc ) cần dùng để điều chế 2,32g từ oxit sắt từ ( Fe=56, O=16)
Bài 4: Đốt chảy 6,2g P đỏ trong bình chứa 6,72 lít khí oxi ( ở đktc ) tạo thành P2O5
a) Chất nào còn dư, chất nào thiếu
b) Khối lượng chất tạo thành là bao ? ( P=31, O=16)

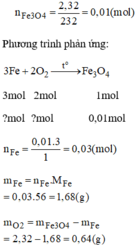

Bài 3 :
PTHH : \(6Fe+4O_2\left(t^o\right)->2Fe_3O_4\) (1)
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{2,32}{56.3+16.4}=0,01\left(mol\right)\)
Từ (1) => \(3n_{Fe_3O_4}=n_{Fe}=0,03\left(mol\right)\)
=> \(m_{Fe}=n.M=1,68\left(g\right)\)
Từ (1) => \(2n_{Fe_3O_4}=n_{O_2}=0,02\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=n.22,4=0,448\left(l\right)\)
Bài 4 :
PTHH : \(4P+5O_2\left(t^o\right)->2P_2O_5\) (1)
\(n_P=\dfrac{m}{M}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{6,72}{32}=0,21\left(mol\right)\)
Có : \(n_P< n_{O_2}\left(0,2< 0,21\right)\)
-> P hết ; O2 dư
Từ (1) -> \(\dfrac{1}{2}n_P=n_{P_2O_5}=0,1\left(mol\right)\)
=> \(m_{P_2O_5}=n.M=14,2\left(g\right)\)
Bài 3:
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
PTHH: 3Fe + 2O2 ---to→ Fe3O4
Mol: 0,03 0,02 0,01
\(m_{Fe}=0,03.56=1,68\left(g\right);V_{O_2}=0,02.22,4=0,448\left(l\right)\)