cho dx/h2=8,5 và dx/y =0,5 tìm khối lượng mol cua khi x va khí y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khối lượng mol khí X là
\(d_{\dfrac{x}{H_2}}=\dfrac{M_x}{M_{H_2}}=8,5\Rightarrow M_x=8,5.2=17\left(gmol\right)\)
Khối lượng mol khí Y là
\(d_{\dfrac{x}{y}}=\dfrac{M_X}{M_Y}=\dfrac{17}{M_Y}=0,5\Rightarrow M_Y=17:0,5=34\left(gmol\right)\)

\(M_X=\dfrac{M_{O_2}}{d_{O_2/x}}=\dfrac{32}{2}=16(g/mol)\\ M_Y=\dfrac{M_X}{d_{X/Y}}=\dfrac{16}{8}=2(g/mol)\)

Hỗn hợp khí X gồm CO và CO2
nX = 0,5 = a + b (1)
Sử dụng sơ đồ đường chéo ⇒ n CO= 0,3 ; n CO2 = 0,2
n CO2 = n O oxit = 0,2 mol
Gọi n là hóa trị của M ⇒ Oxit: M2On
n Fe : n O = 11,2/M : 0,2 = 2 : n ⇒ M = 28n
⇒ n = 2 và M(56) ⇒ FeO
Đáp án C.

Đáp án D
hhX gồm C2H2 và H2 có cùng số mol.
hhX cho qua xúc tác nung nóng
→ hhY gồm C2H4, C2H6, C2H2 và H2.
Sục Y vào brom dư
→ mbình tăng = 19 gam và 0,2 mol hh khí có d/H2 = 8,5.
• Theo BTKL:
mhhX = mbình brom tăng + mkhí thoát ra
= 19 + 0,2 x 17 = 22,4 gam.
→ nC2H2 = nH2 = 22,4 : (26 + 2) = 0,8 mol.
• C2H2 + 2,5O2 → 2CO2 + H2O
0,8----------2
H2 + 0,5O2 → H2O
0,8----0,4
→ ∑nO2 = 2 + 0,4 = 2,4 mol
→ VO2 = 2,4 x 22,4 = 53,76 lít

Chọn đáp án D
Ta có mZ = 0,2 × 8,5×2 = 3,4 gam.
Ta có sơ đồ
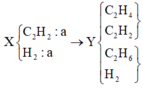
+ Theo định luật BTKL ⇒ mC2H2 + mH2 = 19 + 3,4 = 22,4 gam
⇒ nC2H2 = nH2 = 22,4 ÷ (26 + 2) = 0,8 mol
+ Vì thành phần nguyên tố C và H trong X và Y như nhau.
⇒ Đốt cháy hoàn toàn hh Y hay X thì đều cần 1 lượng oxi như nhau.
Ta có sơ đồ đốt cháy
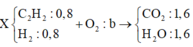
⇒nO2 = b = nCO2 + ½ nH2O = 2,4 mol ⇒ VO2 = 53,76 lít ⇒ Chọn D

Chọn đáp án D
Ta có mZ = 0,2 × 8,5×2 = 3,4 gam.
Ta có sơ đồ

+ Theo định luật BTKL ⇒ mC2H2 + mH2 = 19 + 3,4 = 22,4 gam
⇒ nC2H2 = nH2 = 22,4 ÷ (26 + 2) = 0,8 mol
+ Vì thành phần nguyên tố C và H trong X và Y như nhau.
⇒ Đốt cháy hoàn toàn hh Y hay X thì đều cần 1 lượng oxi như nhau.
Ta có sơ đồ đốt cháy
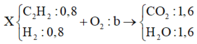
⇒nO2 = b = nCO2 + ½ nH2O = 2,4 mol ⇒ VO2 = 53,76 lít ⇒ Chọn D
\(d_{\dfrac{X}{H_2}}=8,5\\ M_{H_2}=2\\ \Rightarrow M_X=d_{\dfrac{X}{H_2}}.M_{H_2}=8,5.2=17\left(g\right)\)
\(d_{\dfrac{X}{Y}}=0,5\\ \Rightarrow d_{\dfrac{Y}{X}}=2\\ M_X=17\\ \Rightarrow M_Y=d_{\dfrac{Y}{X}}.M_X=2.17=34\left(\dfrac{g}{mol}\right)\)
Ta có: dx/h2 = 8,5
=> Mx = 8,5 . 2 = 17 (g/mol)
dx/y = 0,5
=> My = \(\dfrac{17}{0,5}\) = 34 (g/mol)
Vậy Mx = 17 (g/mol)
My = 34 (g/mol)