điện phân hoàn toàn (dùng điện cực trơ) 4 lit dung dịch muối sun fat kim loại hóa trị III với cường độ dòng điện là 6A. Sau 2,68056 giờ thấy khối lượng catot tăng 11,2 gam.Muối sun fat đã điện phân là muối của kim loại nào? Tính pH của dung dịch thu được, biết thể tích dung dịch không đổi
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Theo định luật Faraday ta có khối lượng chất thoát ra ở điện cực là :
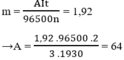
Trong đó A là nguyên tử khối
A = 64 ⇒ A là Cu

\(a.Catot:M^{2+}+2e\rightarrow M\\ Anot:2H_2O\rightarrow4H^++O_2+4e\\ PTHH:2MSO_4+2H_2O-^{đp}\rightarrow2M+O_2+2H_2SO_4\\ b.m=\dfrac{AIt}{nF}=\dfrac{A.3.1930}{2.96500}=1,92\\ \Rightarrow A=64\left(Cu\right)\)

Đáp án A
Quá trình điện phân: M2+ + 2e → M
Có: ne = I.t/F = 3.1930/96500 = 0,06 mol
=> nM = ½ ne = 0,03 mol
=> MM = 1,92: 0,03 = 64 (g/mol) => Cu

Đáp án C
Dạng thời gian t, 2t kết hợp với khối lượng dung dịch giảm. ► quy cái này giải cho dễ này:
dung dịch giảm MO hay M2O hay M2O3 quy hết về dạng MnO nhé (n = 1 hoặc 2 hoặc 2/3 tùy).
• xét thời gian t (giây): dung dịch giảm x mol MnO ⇄ 6,96 gam → ne trao đổi = 2x mol.
thời gian 2t (giây) → ne trao đổi = 4x mol; catot ra 0,01 mol H2 → ứng với dung dịch ra 0,01 mol H2O.
→ 11,78 gam dung dịch giảm gồm 0,01 mol H2O và còn (2x – 0,01) mol MnO nữa.
→ Phương trình: 11,78 = 0,01 × 18 + 2 × 6,96 – 0,01 × MMnO → MnO = 232.
→ nM = 216 ứng với cặp n = 2 và M = 108 là kim loại Ag.
Thay ngược lại → x = 6,96 ÷ 232 = 0,03 mol → a = 6,48 gam


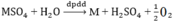
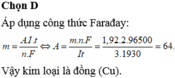
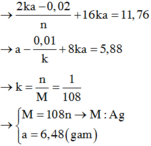
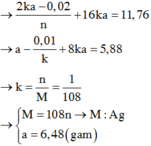
Có \(m=\dfrac{AIt}{nF}=\dfrac{A.6.9650}{3.96500}=11,2=>A=56\left(g/mol\right)\)
=> Muối đã điện phân là Fe2(SO4)3