Ion nào sau đây có nhiều electron nhất
A. SO42-. B. CO32-. C. NO3-. D. NH4+.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Dùng Ba(NO3)2 thì:
CO32-+ Ba2+ → BaCO3 ↓
2PO43- + 3Ba2+→ Ba3(PO4)2
SO42-+ Ba2+ → BaSO4
Khi đó trong dung dịch chỉ còn anion NO3-

NO3- có 6 e-
SO42- có 8e-
CO32- có 6e-
Br không có e
NH4+ có 4e-
Khí hiệu E là số e chứa trong 1 nguyên tử.
- NO3- nghĩa là NO3 nhận thêm 1e
=> số e = EN + 3EO + 1 = 7+3*8+1= 32
- NH4+ là NH4 mất đi 1e
=> số e = EN + 4EH -1 = 7 + 4 - 1 = 10
Các ý còn lại e làm tương tự nhé

Đáp án B
Để dung dịch tồn tại thì các ion không phản ứng với nhau và định luật bảo toàn được thỏa mãn. Ở đây chỉ có đáp án B thỏa mãn.

Trong ion:
NO3-: x + 3.(-2) = -1 ⇒ x = 5 ⇒ N có số oxi hóa là +5 trong hợp chất NO3-.
SO42-: x + 4.(-2) = -2 ⇒ x = 6 ⇒ S có số oxi hóa là +6.
CO32-: x + 3.(-2) = -2 ⇒ x = 4 ⇒ C có số oxi hóa là +4.
Br-: Br có số oxi hóa là -1
NH4+: x + 4 = 1 ⇒ x = -3 ⇒ N có số oxi hóa là -3.

a) Số oxi hóa của Mn trong $KMnO_4$ là $+7$
Số oxi hóa của Cr trong $Na_2Cr_2O_7$ là $+6$
Số oxi hóa của $Cl$ trong $KClO_3$ là $+5$
Số oxi hóa của $P$ trong $H_3PO_4$ là $+5$
b)
Số oxi hóa của $N$ trong $NO_3^-$ là $+5$
Số oxi hóa của $S$ trong $SO_4^{2-}$ là $+6$
Số oxi hóa của $C$ trong $CO_3^{2-}$ là $+4$
Số oxi hóa của $Br$ trong $Br^-$ là $-1$
Số oxi hóa của $N$ trong $NH_4^+$ là $-3$

Đáp án D.
Số hạt e trong các nguyên tử N (e = 7), H (e = 1), O (e = 8), S (e = 16), C( e = 6).
Phân tử NO3-: số e = eN + eO.3 + 1 =32 do NO3- đã nhận thêm 1e
Phân tử NH4+: số e = eN + eH .4 -1 = 10 do NH4+ đã nhường đi 1 e
Phân tử HCO3-: số e = eH + eC + eO.3 + 1 = 32
Phân tử H+: số e = 0
Phân tử SO42-: eS + eO.4 + 2 = 50
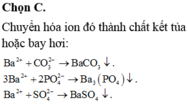
\(A.SO_4^{2-}\)