Cho 9,6g Cu tác dụng với 180 ml dung dịch HNO3 1M thu được V1 lit khí NO duy nhất và dung dịch A. Mặt khác cũng cho lượng Cu như trên tác dụng với 180 ml dung dịch hỗn hợp gồm HNO3 1M và H2SO4 0,5M thì được V2 lit NO duy nhất và dung dịch B.
b) Cô cạn dung dịch B rồi nung nóng đến khối lượng không đổi được m(g) chất rắn. Tính m
c) Oxi hóa V1 lit NO bằng O2 rồi dẫn sản phẩm vào 200ml nước có hòa tan 0,72g khí O2. Tính pH dung dịch sau phản ứng (coi thể tích dung dịch không đổi)

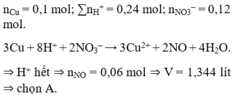
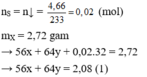
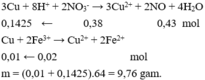
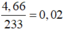
\(n_{Cu}=\dfrac{9,6}{64}=0,15\left(mol\right)\)
\(n_{HNO_3}=0,18\left(mol\right)\)
\(+TH_1:\)
Vì thu được \(NO\) duy nhất → Có 2 trường hợp xảy ra, hoặc là `Cu` hết hoặc là `HNO_3` hết
\(\left[e\right]:2.0,15=3.n_{NO}\Leftrightarrow n_{NO}=0,1\left(mol\right)\)
Mặt khác ta có: \(n_{H^+}=4n_{NO}=0,18\Leftrightarrow n_{NO}=0,045\left(mol\right)\)
→ Chứng tỏ `Cu` dư
\(NO\left(0,045\right)\underrightarrow{+O_2}NO_2\rightarrow HNO_3\)
\(PTHH:NO_2+\dfrac{1}{2}O_2+H_2O\rightarrow2HNO_3\)
\(\left(mol\right)\) \(0,045\) \(0,0225\)
→ Tính theo oxi
\(\Rightarrow n_{HNO_3}=0,0225.2.2=0,09\left(mol\right)\\ \Rightarrow\left[H^+\right]=\dfrac{0,09}{0,2}=0,45\left(M\right)\\ \Rightarrow pH=-log\left(H^+\right)\approx0,35\)
\(+TH_2:\) Tóm tắt các phản ứng như sau
\(0,15\left(mol\right)Cu+\left\{{}\begin{matrix}H_2SO_4:0,09\left(mol\right)\\HNO_3:0,18\left(mol\right)\end{matrix}\right.\rightarrow V\left(l\right)NO+B\left\{{}\begin{matrix}Cu\left(NO_3\right)_2:0,135\\SO_4^{2-}:0,09\end{matrix}\right.+Cu:0,015\left(mol\right)\)
Tương tự như trường hợp 1 ta có:
\(n_{H^+}=4n_{NO}\Leftrightarrow0,36=4n_{NO}\Leftrightarrow n_{NO}=0,09\left(mol\right)\) và \(Cu\) dư \(0,015\left(mol\right)\)
\(\left\{{}\begin{matrix}0,045\left(mol\right)Cu\left(NO_3\right)_2\\0,09\left(mol\right)CuSO_4\end{matrix}\right.+Cu\left(0,015\right)\underrightarrow{t^o}\left\{{}\begin{matrix}CuO:0,045\\CuSO_4:0,09\\Cu:0,015\end{matrix}\right.\)
\(\rightarrow m=0,45.80+0,09.160+0,015.64=18,96\left(g\right)\)