Đốt cháy hoàn toàn m gam cacbon trong V lít O2 (đkc) lấy dư thu được hỗn hợp A có dA/H2=1,25. Cho A qua dd Ca(OH)2 dư thu được 6 gam kết tủa. Tính m và V?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1/
\(2C\left(\dfrac{m}{12}\right)+O_2\left(\dfrac{m}{24}\right)\rightarrow2CO_2\left(\dfrac{m}{12}\right)\)
\(CO_2\left(\dfrac{m}{12}\right)+Ca\left(OH\right)_2\rightarrow CaCO_3\left(\dfrac{m}{12}\right)+H_2O\)
Nếu như O2 thì tỷ khối của hỗn hợp so với O2 phải là: \(\dfrac{44}{32}=1,375>1,25\) vậy trong hỗn hợp khí phải có O2
\(n_C=\dfrac{m}{12}\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{V}{22,4}-\dfrac{m}{12}\left(mol\right)\)
\(\Rightarrow\dfrac{44.\dfrac{m}{12}+32.\left(\dfrac{V}{22,4}-\dfrac{m}{24}\right)}{\dfrac{m}{12}+\dfrac{V}{22,4}-\dfrac{m}{24}}=1,25.32=40\)
\(\Leftrightarrow15V-28m=0\left(1\right)\)
Ta lại có: \(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
\(\Rightarrow\dfrac{m}{12}=0,06\Leftrightarrow m=0,72\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}15V-28m=0\\m=0,72\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m=0,72\left(g\right)\\V=1,344\left(l\right)\end{matrix}\right.\)

\(M_X = 18.2 = 36(đvC)\)
X gồm CO2,CO
Ta có :
\(44n_{CO_2} + 28n_{CO} = 36(n_{CO_2} + n_{CO})\\ \Rightarrow 8n_{CO_2} = 8n_{CO}\\ \Rightarrow n_{CO_2} = n_{CO}\)
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
Theo PTHH :
\(n_{CO} = n_{CO_2} = n_{CaCO_3} = \dfrac{20}{100} = 0,2(mol)\)
\(C + O_2 \xrightarrow{t^o} CO_2\\ 2C + O_2 \xrightarrow{t^o} 2CO\\ n_{O_2} = n_{CO_2} + \dfrac{n_{CO}}{2} = 0,3(mol)\\ \Rightarrow V = 0,3.22,4 = 6,72(lít)\)
\(\)

\(n_{Ba\left(ỌH\right)_2}=0,1.0,3=0,03\left(mol\right)\\ n_{BaCO_3}=\dfrac{3,94}{197}=0,02\left(mol\right)\)
PTHH:
Ba(OH)2 + CO2 ---> BaCO3 + H2O
0,02 0,02 0,02
So sánh: 0,2 < 0,3 => Có tạo muối axit
\(n_{Ba\left(OH\right)_2\left(tạo.muối.axit\right)}\) = 0,03 - 0,02 = 0,01 (mol)
Ba(OH)2 + CO2 + H2O ---> Ba(HCO3)2
0,01 0,01
=> nCO2 = 0,02 + 0,01 = 0,03 (mol)
PTHH: C + O2 ---to---> CO2
0,03 0,03 0,03
mC = 0,03.12 = 0,36 (g)
=> m = mthan = \(\dfrac{0,36}{100\%-4\%}=0,375\left(g\right)\)
Gọi nO2 (dư) = a (mol)
=> \(M_A=\dfrac{0,03.44+32a}{0,03+a}=19,6.2\\ \Leftrightarrow a=0,02\left(mol\right)\)
=> VO2 = (0,03 + 0,02).22,4 = 1,12 (l)



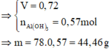
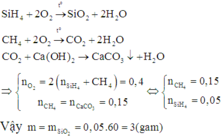
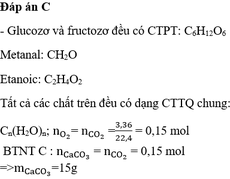
A gồm hai khí CO(M = 28), CO2(M = 44)
Suy ra: \(28< M_A < 44\)
Mà theo đề bài : \(M_A = M_{H_2} .1,25 = 2.1,25 = 2.5\)
→ Sai đề
C + O2 -to-> CO2
CO2 + Ca(OH)2 -> CaCO3 + H2O
nCaCO3=0,06(mol) ->nC= nCO2=0,06(mol)
=> m=mC=0,06.12=0,72(g)
dA=H2=1,25 -> M(A)=2,5 ???
Nhỏ hơn cả M(O2) và M(CO2), anh nghĩ là đề có nhầm lẫn. Em xem lại nhé!