Cho 12g NaOH trong dd 100ml dd H2SO4 1M vừa đủ thu dd A. Tính khối lượng chất rắn khan thu được sau khi cô cạn dung dịch A?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Cho hh 2 muối tác dụng với H2SO4 loãng
MgCO3 + H2SO4 → MgSO4 + H2O + CO2
RCO3 + H2SO4 → RSO4 + H2O + CO2
Số mol khí CO2 sinh ra: n(CO2 1) = 4,48/22,4 = 0,2mol
Nung chất rắn không tan sau pư thấy thoát ra khí CO2 → muối cacbonat dư → H2SO4 đã tham gia phản ứng hết.
Số mol H2SO4 đã dùng: n(H2SO4) = n(CO2) = 0,2mol
Nồng độ dung dịch H2SO4: C(H2SO4) = 0,2/0,5 = 0,4M
b./ Theo ĐL bảo toàn khối lượng:
m(hh muối) + m(H2SO4) = m(muối khan) + m(B) + m(CO2) + m(H2O)
→ m(B) = m(hh muối) + m(H2SO4) - m(muối khan) - m(CO2) - m(H2O) = 115,3 + 0,2.98 - 12.2 - 0,2.44 - 0,2.18 = 110,3g
c./ Số mol CO2 thu được khi nung B: n(CO2 2) = 11,2/22,4 = 0,5mol
Tổng số mol hai muối:
n(hh muối) = n(MgCO3) + n(RCO3) = n(CO2 1) + n(CO2 2) = 0,2 + 0,5 = 0,7mol
n(RCO3) = 2,5.n(MgCO3) → n(MgCO3) = 0,2mol và n(RCO3) = 0,5mol
Khối lượng mỗi muối:
m(MgCO3) = 84.0,2 = 16,8g
m(RCO3) = m(hh muối) - m(MgCO3) = 115,3 - 16,8 = 98,5g
Khối lượng mol phân tử của muối cacbonat cần tìm:
M(RCO3) = R + 60 = m(RCO3)/n(RCO3) = 98,5/0,5 = 197
→ R = 137
Vậy kim loại cần tìm là Ba.

Đáp án C
nNaOH = 0,5 mol
nH2SO4 = 0,35 mol
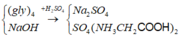
Bảo toàn nguyên tố Na : nNa2SO4 = 0,25 mol
Bảo toàn nguyên tố S → nmuối hữu cơ = 0,35-0,25=0,1 mol
→m = 0,25.142 + 0,1.248=60,3 g

nH2= 2.24: 22.4 = 0,1(mol)
nNaAlO2= 16,4:82=0,2(mol)
Gọi nAl=a (mol;a>0)
nNaAlO2= b (mol; b>0)
(1) Al + NaOH + H2O --> NaAlO2 + 3/2 H2
Ta có a a a 1,5a (mol)
(2) Al2O3 + 2NaOH --> 2NaAlO2 + H2O
Ta có b 2b (mol)
Ta có nH2 = 0,1 (mol) => 1,5a = 0,1 => a = 2/30=>nAl = 2/30(mol)
nNaAlO2 = 0,2(mol) =>a+2b=0,2=> b=??
Còn lại bn tự làm nha!!!!!!!!
Có chỗ nào sai mong mọi người thông cảm:))

10) Tham Khảo
Gọi x là nHCl, y là nH2SO4
nNaOH=0.5.0.04=0.02mol
=>nOH-=0.02mol
PT:
H(+)+OH(-)-->H2O
0.02<0.02
=>nH+ trong 10ml hh axit=0.02
=>nH+ trong 100ml hh axit=0.02.10=0.2mol
PT:
H(+)+OH(-)-->H2O
0.2->0.2
=>nNaOH=0.2mol
m muối=mNa(+)+mCl(-)+mSO4(2-)=23.0.2+35.5x...
< = > 35.5x+96y=8.6 (1)
Ta lại có: nH+=x+2y=0.2 (2)
Từ (1)(2)=>x=0.08, y=0.06.
Vậy [HCl]=0.08M, [H2SO4]=0.06M.

mCuO giảm= mO
H2+ O -> H2O
=> nH2= nO= 0,35 mol
=> nCl= nHCl= 2nH2= 0,7 mol
m= m kim loại+ mCl= 14,8+ 0,7.35,5= 39,65g
mCuO giảm= mO
H2+ O -> H2O
=> nH2= nO= 0,35 mol
=> nCl= nHCl= 2nH2= 0,7 mol
m= m kim loại+ mCl= 14,8+ 0,7.35,5= 39,65g

$MgCO_3 + H_2SO_4 \to MgSO_4 +C O_2 + H_2O$
$RCO_3 + H_2SO_4 \to RSO_4 +C O_2 + H_2O$
Theo PTHH :
$n_{H_2SO_4} = n_{CO_2} = 0,2(mol)$
$\Rightarrow C_{M_{H_2SO_4}} = \dfrac{0,2}{0,5} = 0,4M$
Theo PTHH : $n_{H_2O} = n_{H_2SO_4} = 0,2(mol)$
Bảo toàn khối lượng : $m_B = 115,3 + 0,2.98 - 0,2.44 -0,2.18 -12=110,5(gam)$
$m_B = m_B - m_{CO_2} = 110,5 - 0,5.44 = 88,5(gam)$
Gọi $n_{MgCO_3} =a (mol) \Rightarrow n_{RCO_3} = 2,5a(mol)$
Bảo toàn nguyên tố C :
$a + 2,5a = 0,5 + 0,2 \Rightarrow a = 0,2(mol)$
Ta có :
$0,2.84 + 0,2.2,5.(R + 60) = 115,3 \Rightarrow R = 137(Bari)$
\(n_{NaOH}=\dfrac{12}{40}=0.3\left(mol\right)\)
\(n_{H_2SO_4}=0.1\cdot1=0.1\left(mol\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(0.2..............0.1................0.1\)
\(m_A=m_{Na_2SO_4}+m_{NaOH\left(dư\right)}=0.1\cdot142+\left(0.3-0.2\right)\cdot40=18.2\left(g\right)\)