Đốt cháy hoàn toàn 122 lít (đktc) hiđrô với lượng khí oxi dư. Hỏi thu được thể tích nước ở trạng thái lỏng là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


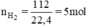
Phương trình phản ứng tổng hợp nước:
2H2 + O2 → 2H2O.
Theo pt: nH2O = nH2 = 5mol.
mH2O= 5.18 = 90g.
Khối lượng riêng của nước là 1g/ml thể tích nước lỏng thu được là 90ml.

\(n_{H_2}=\dfrac{112}{22,4}=5\left(mol\right)\)
Bảo toàn nguyên tố H : \(n_{H_2}.2=n_{H_2O}.2\)
=> nH2O =5(mol)
=> m H2O = 5.18= 90(g)

\(a) 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ n_{H_2O} = \dfrac{1,8}{18} = 0,1(mol)\\ n_{H_2} = n_{H_2O} = 0,1 \Rightarrow V_{H_2} = 0,1.22,4 = 2,24(lít)\\ V_{O_2} = \dfrac{1}{2}V_{H_2} = 1,12(lít)\\ b) n_{H_2O} = n_{H_2} = \dfrac{112}{22,4} = 5(mol)\\ \Rightarrow m_{H_2O} = 5.18 = 90(gam)\)

a)
SO3 + H2O $\to$ H2SO4
n H2SO4 = n SO3 = 240/80 = 3(mol)
m H2SO4 = 3.98 = 294(gam)
b)
2H2 + O2 $\xrightarrow{t^o}$ 2H2O
V H2 / 2 = 0,56 < V O2 = 1,68 nên O2 dư
n H2O = n H2 = 1,12/22,4 = 0,05(mol)
m H2O = 0,05.18 = 0,9(gam)
V H2O = m/D = 0,9/1 = 0,9(ml)
c)
n NaOH = 16/40 = 0,4(mol)
Na2O + H2O $\to$ 2NaOH
n Na2O = 1/2 n NaOH = 0,2(mol)
m Na2O = 0,2.62 = 12,4(gam)
a)Ta có PT:SO4+H2O=H2SO4
Theo bài ra t có nSO4=240:96=2,5
Mà nSo4=nH2So4=2,5 mol
suy ra:mH2So4=2,5.98=245g
