Khi hòa tan 2,75 gam hỗn hợp Zn và CuO trong 200 ml dd HNO3 (x) M lấy dư thu được 448ml NO (đktc) duy nhất. Khối lượng CuO trong hỗn hợp và giá trị của x là:
A. 0,8g; 0,5M. B. 1,95g; 0,05M.
C. 0,8g; 0,4M. D. 1,2g; 0,3M.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Sơ đồ quá trình phản ứng:
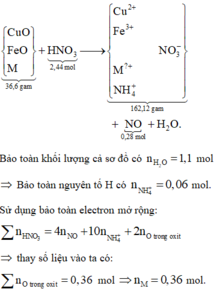
(sự đặc biệt của nguyên tố O trong các oxit, n O = n FeO + n CuO ). Dùng bảo toàn electron thường, ta có:


Đáp án : B
Z có : nCO = nCO2 = 0,03 mol
=> nO pứ = nCO pứ = 0,03 mol. Đặt nO dư = a
=> Coi Y gồm Kim loại và O dư a mol
=> m = (100/25).16(a + 0,03) = 64(a + 0,03)
=> nNO3 muối = 2a + 0,04.3 = 2a + 0,12 mol
=> 3,08.64(a + 0,03) = [64(a + 0,03) – 16(a + 0,03)] + 62(2a + 0,12)
=> a = 0,118 => m = 64( 0,118 + 0,03) = 9,472g

Đáp án B
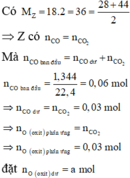
Quy đổi hỗn hợp Y tương ứng với hỗn hợp gồm các kim loại và O dư (a mol)
Có m O = 16 . ( a + 0 , 3 ) gam ⇒ m = 64 a + 1 , 92 ( 1 )
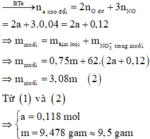
Vậy m gần với giá trị 9,5 nhất

Đáp án A
· Quy đổi X tương đương với hỗn hợp gồm Al, Fe, Cu và x mol O
![]()
· Khí Z gồm CO2 (a mol) và CO dư (b mol)
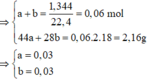
Y + HNO3 → 3,08m g muối + 0,04 mol NO


Đáp án : A
Hỗn hợp Z gồm CO và CO2 có M = 36 dùng đường chéo => tỷ lệ mol CO = CO2 = 0,03 mol
Số mol O phản ứng = CO = 0,03 mol nên số mol O còn trong Y = (0,25m/16 - 0,03)
Khối lượng kim loại trong Y : 0,75m.
Khi phản ứng với HNO3 tạo muối có 2 loại: NO3- tạo muối thay thế O2- là 2(0,25m/16 - 0,03)(không tạo sp khử) và NO3- tạo muối có sp khử:
Số mol NO3- tạo muối tính theo NO = 0,04.3 = 0,12 mol
áp dụng BTKL: 3,08m = 0,75m + 62.0,12 + 62.2(0,25m/16 - 0,03)
=> m = 9,477 gần giá trị 9,5.
\(Zn\rightarrow Zn^{2+}+2e\\ 4H^++NO_3^-+3e\rightarrow NO+2H_2O\\ CuO+HNO_3\rightarrow Cu\left(NO_3\right)_2+H_2O\\ n_{NO}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\\ BTe:n_{Zn}.2=n_{NO}.3\\ \Rightarrow n_{Zn}=0,03\left(mol\right)\\ \Rightarrow m_{CuO}=2,75-0,03.65=0,8\left(g\right)\\ \Rightarrow n_{CuO}=\dfrac{0,8}{80}=0,01\left(mol\right)\\ n_{HNO_3}=n_{NO}.4+n_{CuO}.2=0,1\left(mol\right)\\ \Rightarrow CM_{HNO_3}=\dfrac{0,1}{0,2}=0,5M\\ \Rightarrow ChọnA\)