Tính khối lượng bari sunsat tạo thành khi cho 3,12 gam bariclorua phản ứng với 5,68 gam natri sunfat ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Bari clorua + Natri sunfat → Bari sunfat + Natri clorua
b) mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
c) Tổng khối lượng các chất sau phản ứng là: 350g
d) mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
⇔208 + 142 = 233 + mNaCl
⇒mNaCl= 117(g)
e) Khi phản ứng xảy ra có 137g nguyên tử Bari, thì sau phản ứng sẽ có 137g nguyên tử Bari.
f) Khi phản ứng thu được 71g nguyên tử Clo, thì trước phản ứng đã có 71g nguyên tử Clo tham gia phản ứng.

Phương trình chữ của phản ứng:
Natri sunfat + Bari clorua → Bari sunfat + Natri clorua
Theo định luật bảo toàn khối lượng
mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
⇒ mBaCl2 = mBaSO4 + mNaCl - mNa2SO4 = 23,3 + 11,7 - 14,2 = 20,8g.

a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\)
Vậy \(Al\left(OH\right)_3\) dư.
\(m_{dư}=0,75.78-98.0,5=9,5\left(g\right)\)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,5=\dfrac{1}{6}\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)

a, \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right);n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
PTHH: 2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
Mol: \(\dfrac{1}{3}\) 0,5 \(\dfrac{1}{6}\)
b, Ta có: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\) ⇒ Al(OH)3 dư, H2SO4 hết
⇒ \(m_{Al\left(OH\right)_3}=\left(0,75-\dfrac{1}{3}\right).78=32,5\left(g\right)\)
c, \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)
Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Không có chất dư (hoặc có thể bn cho sai 49(g) dung dịch là 49(g) H2SO4)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al\left(OH\right)_3}=\dfrac{1}{2}.0,75=0,375\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,375.342=128,25\left(g\right)\)

Sơ đồ
Sắt (III) sunfat + Natri hidroxit → Sắt (III) hidroxit + natri sunfat
Áp dụng ĐLBTKL, ta có
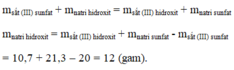

\(n_{Ba\left(OH\right)_2}=\dfrac{17,1}{171}=0,1\left(mol\right)\)
\(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\)
0,1 -----------> 0,1------------>0,1----------> 0,2
\(m_{NaOH}=0,2.40=8\left(g\right)\)
\(m_{BaSO_4}=0,1.233=23,3\left(g\right)\)
C1: \(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
c2: theo đlbtkl \(m_{Na_2SO_4}=23,3+8-17,1=14,2\left(g\right)\)
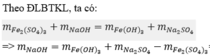

\(n_{BaCl_2}=\dfrac{3,12}{208}=0,015\left(mol\right)\\ m_{Na_2SO_4}=\dfrac{5,68}{142}=0,04\left(mol\right)\\ PTHH:BaCl_2+Na_2SO_4\rightarrow BaSO_4+2NaCl\)
Lập tỉ lệ \(\dfrac{n_{BaCl_2}}{1}=0,015< \dfrac{m_{Na_2SO_4}}{1}=0,04\)
=> BaCl2 hết Na2So4 dư
Theo pt ta có:
\(n_{BaSO_4}=n_{BaCl_2}=0,015\left(mol\right)\\ m_{BaSO_4}=0,015.233=3,495\left(g\right)\)