Cho một miếng Na tác dụng hoàn toàn với 100ml dung dịch AlCl3 x (mol/l), sau phản ứng thu được 5,6 lít khí ở đktc và một lượng kết tủa. Lấy kết tủa đem nung đến khối lượng không đổi thu được 5,1g chất rắn. Giá trị của x là :
A. 1,1
B. 1,3
C. 1,2
D. 1,5



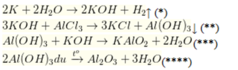

Đáp án : D
nAl2O3 = 0,05 mol => nAl(OH)3 = 0,1 mol
, nH2 = 0,25 mol
,nNa = nNaOH = 2nH2 = 0,5 mol
=> Kết tủa bị tan 1 phần => nAl(OH)3 = 4nAl3+ - nOH-
=> x = 1,5(M)