Đốt cháy hoàn toàn m gam FeS2 bằng O2 dư, thu được khí X. Hấp thụ hết X vào dung dịch Ba(OH)2 dư sau phản ứng hoàn toàn thu được 43,4 gam kết tủa. Giá trị của m là:
A. 12,0
B. 13,2.
C. 24,0.
C. 24,0.0
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
Bảo toàn S : nBaSO3 = nSO2 = 2nFeS2 = 0,2 mol
=> nFeS2 = 0,1 mol => m = 12g

Đáp án C.
nBa(OH)2= 0,1.2 = 0,2 (mol); nBaSO3 = 0,1 (mol)
nBaSO3 = 2 nBa(OH)2 - nSO2 ⇒ nSO2 = 2.0,2 – 0,1 = 0,3 (mol)
FeS2 → 2SO2 (Bảo toàn S)
0,15 0,3 (mol)
⇒ mFeS2 = 0,15.(56+32.2) = 18 (g)

Chọn đáp án D
Các chất trong X đều có CTPT là C4H8O2 và M = 88. nX = 0,075 mol.
Sơ đồ đốt: C4H8O2 → 4CO2 + 4H2O.
n C O 2 = n H 2 O = 4 n X = 0 , 3 m o l
m = 0,3.197 = 59,1 gam.
∆m = mdd sau = mdd trước = m2 - m1 = m C O 2 + m H 2 O – m
= 0,3.(44 + 18) – 59,1
= –40,5

Đáp án D
4FeS2 +11O2 2Fe2O3 +8SO2
![]()
![]()
Vì cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa nên trong Y có
![]()
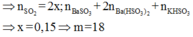
Đáp án D
Chọn đáp án A