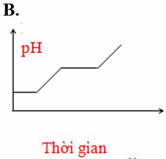
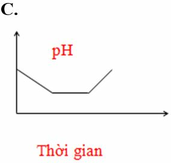
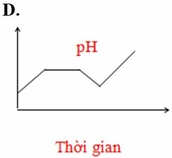
Điện phân dung dịch chứa HCl, NaCl, FeCl3 (điện cực trơ, có màng ngăn). Đồ thị nào sau đây biểu diễn đúng sự biến thiên pH của dung dịch theo thời gian (bỏ qua sự thuỷ phân của muối)?

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
Lúc đầu Fe3+ bị điện phân trước thành Fe2+ nên PH không đổi ⇒ loại C, D.
Sau đó đến H+ bị điện phân nên nồng độ axit giảm ⇒ PH tăng ⇒ B.

Đáp án A
Trên anot xảy ra sự oxi hóa ion , quá trình này không ảnh hưởng đến pH của dung dịch.
Trên catot xảy ra sự khử theo thứ tự ưu tiên như sau :


Đáp án : B
Thứ tự :
Fe3+ + 1e -> Fe2+ ( pH không đổi)
H+ + 1e -> ½ H2 ( pH tăng vì H+ bị điện phân)
Fe2+ + 2e -> Fe ( pH không đổi)
2H2O +2e -> 2OH- + H2 ( pH tăng vì tạo OH-)

Chọn B.
Lúc đầu Fe3+ bị điện phân trước thành Fe2+ nên PH không đổi =>loại C, D.
Sau đó đến H+ bị điện phân nên nồng độ axit giảm => PH tăng => B

Đáp án C.
+ Giai đoạn 1: CuSO4 và NaCl điện phân trước và CuSO4 hết, NaCl còn dư:
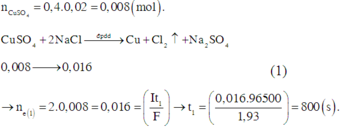
+ Giai đoạn 2: HCl điện phân, nồng độ axit giảm, pH tăng dần từ 2 (ban đầu) đến 7 (khi HCl hết, chỉ còn NaCl và Na2SO4).
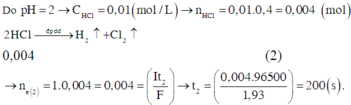
+ Giai đoạn 3: NaCl bị điện phân, nồng độ NaOH tạo thành tăng, pH tăng dần.
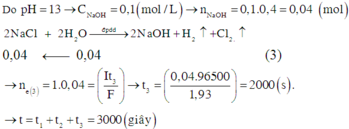
Chọn A