Cho 38,55 gam hỗn hợp X gồm Mg, Al, ZnO và Fe(NO3)2 tan hoàn toàn trong dung dịch chứa 0,725 mol H2SO4 loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa 96,55 gam muối sunfat trung hòa và 3,92 lít (đktc) khí Z gồm hai khí trong đó có một khí hóa nâu ngoài không khí. Biết tỉ khối của Z so với H2 là 9. Phần trăm số mol của Mg trong hỗn hợp X gần nhất với giá trị nào sau đây?
A. 25.
B. 15.
C. 40.
D. 30.

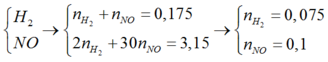
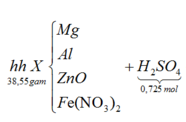
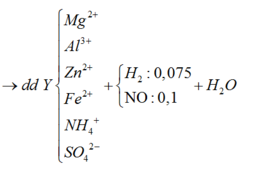


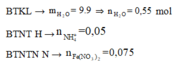




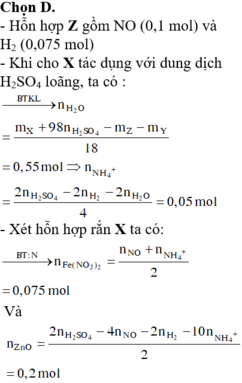




Đáp án D
Khí hóa nâu ngoài không khí là NO.
· Áp dụng bảo toàn khối lượng có:
Có:
=> Chứng tỏ có sản phẩm N H 4 + :
· Áp dụng bảo toàn N có: n F e ( N O 3 ) 2
· Áp dụng bảo toàn nguyên tố O có:
· Đặt số mol của Mg, Al lần lượt là a, b
= 8,85
Vì có sản phẩm H2 tạo thành nên sau phản ứng Fe vẫn ở dạng Fe (II).
Áp dụng bảo toàn electron có:
Suy ra
=>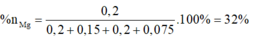
Gần với giá trị 30 nhất.