Nhỏ rất từ từ dung dịch Ba(OH)2 vào dung dịch hỗn hợp chứa đồng thời Al2(SO4)3 và Na2SO4. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa theo số mol Ba(OH)2 như sau:
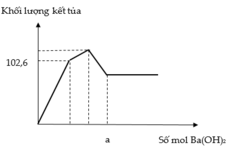
Giá trị của a là?
A. 0,40
B. 0,45
C. 0,48
D. 0,50
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Định hướng tư duy giải
Giai đoạn 1: Tạo đến 102,6 gam kết tủa
là Ba(OH)2 chơi với (x mol) Al2(SO4)3
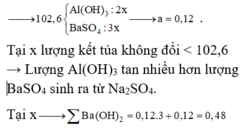

Chọn đáp án C
Giai đoạn 1: Tạo đến 102,6 gam kết tủa Ba(OH)2 chơi với (x mol) Al2(SO4)3.
102 , 6 A l ( O H ) 3 : 2 x B a S O 4 : 3 x → a = 0 , 12
Tại x lượng kết tủa không đổi <102,6 → Lượng Al(OH)3 tan nhiều hơn lượng BaSO4 sinh ra từ Na2SO4.
Tại x → ∑ B a ( O H ) 2 = 0 , 12 . 3 + 0 , 12 = 0 , 48

Đáp án D
Bài này là trường hợp cho Ba(OH)2 vào S O 4 2 - A l 2 S O 4 3
=> điểm cực đại đầu tiên là Al(OH)3 max và điểm cực đại thứ hai là BaSO4 max
- Tại nBa(OH)2 = x thì kết tủa đạt max (BaSO4 đạt max): x = nBa(OH)2 = nBaSO4 max = 69,9: 233 = 0,3 mol

Đáp án A
Tại 69,9 gam kết tủa → Al(OH)3 tan hoàn toàn
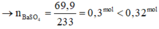
Tại m gam kết tủa → kết tủa tối đa → BaSO4 cực đại → x = 0,3 mol

Đáp án B
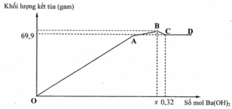
+ Đoạn OA biểu diễn tỉ lệ phản ứng: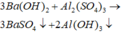
+ Đoạn AB biểu diễn tỉ lệ phản ứng:![]()
+ Đoạn BC biểu diễn tỉ lệ phản ứng:![]() (*)
(*)
+ Đoạn CD, kết tủa chỉ có BaSO4 không thay đổi khi cho thêm Ba(OH)2 dư vào.
Như phân tích trên, 69,9 gam kết tủa tại điểm C là 0,3 mol BaSO4
Xét lại đoặn gấp khúc OAB: x mol Ba đi hết về trong 0,3 mol BaSO4 → x = 0,3.
* Nhận xét: nếu yêu cầu giải rõ hơn số mol các chất, ta giải như sau:
Gọi số moi Na2SO4 và Al2(SO4)3 lần lượt là a, b mol → a + 3b = 0,3 (1)
Cũng tại C, 0,32 mol Ba sẽ đi về 0,3 mol BaSO4 + 0,02 mol Ba(AlO2)2.
Nhưng, đừng vội ẩu vì thật chú ý ở (*), nó nhắc nhở ta rằng, Al đi hết về nhưng không phải vào hết Ba(AlO2)2 mà còn có trong 2a mol NaAlO2 nữa → ∑nnguyên tố Al = 2b = 0,02 × 2 + 2a (2).
Giải hệ các phương trình (1) và (2) được a = 0,06 mol và b = 0,08 mol.