Cho 6,72 gam Fe vào 400 ml dung dịch HNO3 1M, đến khi phản ứng xảy ra hoàn toàn, thu được khí NO (sản phẩm khử duy nhất) và dung dịch X. Dung dịch X có thể hoà tan tối đa m gam Cu. Giá trị của m là
A. 1,92.
B. 3,20
C. 0,64
D. 3,84
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nFe = 0,12 mol → ne cho = 0,36 mol; nHNO3 = 0,4 mol → ne nhận = 0,3 mol
- Do ne cho > ne nhận → Fe còn dư → dung dịch X có Fe2+ và Fe3+
- Các phản ứng xảy ra là:
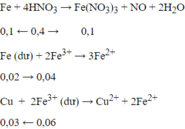
→ mCu = 0,03.64 = 1,92 gam

Đáp án A
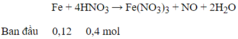
→ HNO3 hết , sau phản ứng có : Fe(NO3)3 0,1 mol ; Fe dư : 0,02 mol
Lượng Cu tối đa đuợc hoà tan hết là khi nó tham gia cả hai phản ứng :
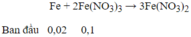
→ Sau phản ứng Fe(NO3)3 dư : 0,1 – 0,04 = 0,06 mol
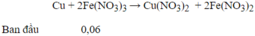
→ Số mol Cu tối đa được hoà tan là : 0,03 mol → m Cu = 0,03.64 = 1,92 gam

Đáp án D
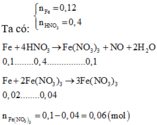
Cu + 2Fe(NO3)3→ Cu(NO3)2+2Fe(NO3)2
0,03 0,06
mCu= 0,03.64 = 1,92(g)

Chọn C
Ta có nFe = 0,12 mol; nHNO3 = 0,4 mol
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
0,1 ← 0,4 → 0,1
(dư 0,02)
Fe còn dư + 2Fe(NO3)3 → 3Fe(NO3)2
0,02 → 0,04
(còn dư 0,06)
Dung dịch X chứa Fe(NO3)2 và Fe(NO3)3 còn dư
Khi cho Cu và dung dịch X thì:
Cu + 2Fe(NO3)3còn dư →Cu(NO3)2 + 2Fe(NO3)2
0,03 ← 0,06
Vậy mCu tối đa = 64.0,03 = 1,92g

nFe = 0,12 mol → ne cho = 0,36 mol; nHNO3 = 0,4 mol → ne nhận = 0,3 mol
- Do ne cho > ne nhận → Fe còn dư → dung dịch X có Fe2+ và Fe3+
- Các phản ứng xảy ra là:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
0,1 ← 0,4 → 0,1
Fe (dư) + 2Fe3+ → 3Fe2+
0,02 → 0,04
Cu + 2Fe3+ (dư) → Cu2+ + 2Fe2+
0,03 ← 0,06
→ mCu = 0,03.64 = 1,92 gam → đáp án A
Coi hỗn hợp Cu và Fe cho vào HNO3
=> 8/3nFe + 8/3nCu = n HNO3 pư = 0,4
=> n Cu = 0,03 mol
=> m Cu = 1,92 gam
D/an :A

Đáp án A
n Fe = 0 , 12 ; n HNO 3 = 0 , 4
Tương tự như Câu 6, trong dung dịch X, gọi
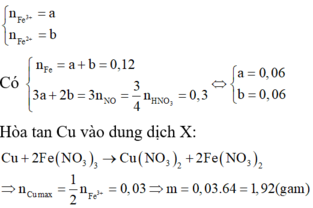
Đáp án A
Số mol Fe=0,12(mol) số mol HNO3=0,4 (mol)
Fe+4HNO3→Fe(NO3)3+NO+2H2O Fe + 2Fe(NO3)3→3Fe(NO3)2
0,1 0,4 0,1 0,02 0,04
Fe(NO3)3 dư =0,1-0,04=0,06(mol)
Cu + 2Fe(NO3)3→Cu(NO3)2+2Fe(NO3)2
0,03 0,06
mCu=0,03.64=1,92(g)