Cho 30,88 gam hỗn hợp gồm Cu và Fe3O4 vào V lít dung dịch HCl 2M được dung dịch X và còn lại 1,28 gam chất rắn không tan. Cho dung dịch AgNO3dư tác dụng với dung dịch X được 0,56 lít khí Y (ở đktc) không màu hoá nâu trong không khí và m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. V và m lần lượt là
A. 5,04 lít và 153,45 gam
B. 0,45 lít và 153,45 gam
C. 5,04 lít và 129,15 gam
D. 0,45 lít và 129,15 gam

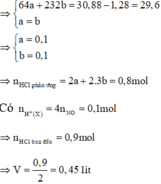






Đáp án : B
Vì X thêm AgNO3 có khí => còn H+ => Fe2O3 hết => chất rắn là Cu
=> Fe3+ -> Fe2+
Fe3O4 + 8HCl -> 2FeCl3 + FeCl2 + 4H2O
2FeCl3 + Cu -> CuCl2 + 2FeCl2
3Fe2+ + 4H+ + NO3- -> 3Fe3+ + NO + 2H2O
Fe2+ + Ag+ -> Fe3+ + Ag
Ag+ + Cl- -> AgCl
Gọi số mol Fe3O4 là x mol => nCu pứ = x mol
=> 232x + 64x + 1,28 = 30,88 => x = 0,1 mol
=> X gồm : 0,3 mol FeCl2; 0,1 mol CuCl2
Ta có : 4nNO = nH+ = 4/3nFe2+ = 0,1 mol => nFe2+ pứ = 0,075 mol
=> nHCl ban đầu = 2nFeCl2 + 2nCuCl2 + nH+ = 0,9 mol => V = 0,45 lit
Fe2+ + Ag+ -> Fe3+ + Ag
=> nkết tủa = mAg + mAgCl = 108.(0,3 – 0,075) + 143,5.0,9 = 153,45g