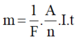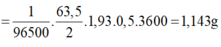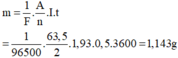Điện phân dung dịch CuSO4 với cực dương là Cu. Biết khối lượng mol của Cu là 64. Cường độ dòng điện chạy qua bình điện phân là 4 A. Lấy F = 96500 (C/mol). Để khối lượng Cu bám ở catot là 1,28g thì cần cho dòng điện chạy qua bình điện phân trong bao lâu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
+ Khối lượng Ag bám ở catot m = A I t F n → I = m F n A t = 6 , 48 . 96500 . 1 108 . 965 = 6 A .

Đáp án B
+ Khối lượng Ag bám ở catot m = A I t F n → I = m F n A t = 6 , 48 . 96500 . 1 108 . 965 = 6 A .

Ta có: m 1 = A 1 I t F n 1 ; m 2 = A 2 I t F n 2 ; m 1 + m 2 = ( A 1 n 1 + A 2 n 2 ) . I t F
⇒ I = ( m 1 + m 2 ) F A 1 n 1 + A 2 n 2 t = 0 , 4 A ; m 1 = A 1 I t F n 1 = 3 , 24 g ; m 2 = m - m 1 = 0 , 96 g

Lời giải:
Ta có khối lượng bạc bám ở cực âm: m = 1 F . A n I t → I = m F n A t = 27.96500.1 108.60.60 = 6 , 7 A
Đáp án cần chọn là: A

Đáp án A. Áp công thức của 2 định luật Faraday suy ra I = m n F A t = 27 . 1 . 96500 108 . 3600 = 6 , 7 A