Trộn lẫn 3 dd H2SO4 0,1M, HNO3 0,2M và HCl 0,3M với những thể tích bằng nhau thu được dd A. Lấy 300 ml dd A cho phản ứng với V lít dd B gồm NaOH 0,2M và KOH 0,29M thu được dd C có pH = 2. Giá trị V là:
A. 0,424 lít
B. 0,214 lít
C. 0,414 lít
D. 0,134 lít



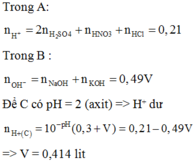
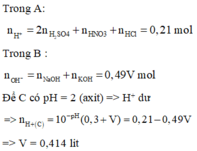
Để có được 300ml dung dịch A thi phải cần mỗi dung dịch axit là 100ml
=> tổng n H+= ( 0,1.2 + 0,2 + 0,3 ). 0,1 = 0,07 mol
Ở dung dịch B có tổng n OH− = 0,49.V mol
rõ ràng dung dịch thu được pH = 2 => dư H^+ = 0,01. ( 0,3 + v ) mol (1)
phản ứng : H+ +OH− → H2O
theo phản ứng thì nH+ dư = 0,07 - 0,49.V (2) từ 1 và 2 => 0,07 - 0,49.V = 0,01. ( 0,3 + v )
=> V = 0,134 lit
=> Đáp án D