Cho hai bình điện phân, bình (I) đựng 20 ml dung dịch NaOH 1,73 M; bình (2) đựng dung dịch gồm 0,225 mol Cu(NO3)2 và 0,2 mol HCl. Mắc nối tiếp bình (1) và bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M. Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất của N+5 .Giá trị m là:
A. 9,8.
B. 9,4.
C. 10,4.
D. 8,3.





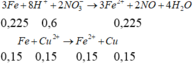

Đáp án D
Ở đây có dùng một kiến thức vật lí:
mắc nối tiếp nên hai bình điện phân cùng I.
• bình (1): giải điện phân NaOH
→ có thể coi là quá trình điện phân H2O
từ CM (NaOH) → nH2O bị điện phân = 0,15 mol ⇄ ne trao đổi = 0,3 mol.
• dùng giả thiết ne trao đổi trên: có điện phân bình (2) ra:
0,1 mol CuCl2 + 0,05 mol CuO.
||→ bảo toàn gốc NO3 đọc ra dd sau điện phân gồm 0,075 mol Cu(NO3)2 và 0,3 mol HNO3.
Quy về giải 0,25 mol Fe + 0,075 mol Cu(NO3)2 + 0,3 mol HNO3
→ ? gam chất rắn không tan.!
Giải: m gam chất rắn gồm 0,075 mol Cu và 0,0625 mol Fe ⇄ m = 8,3 gam.