X là một oxit kim loại trong đó 70% khối lượng là kim loại. Cần bao nhiêu lít dung dịch H2SO4 1M để hòa tan hết 40 gam X?
A. 0,75 lít.
B. 1 lít.
C. 1,25 lít.
D. 0,5 lít.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

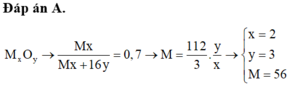
![]()

mk đùa mà cậu đăng thật à >>>> lỡ rồi giúp mk lun nha >>> khỏi nhắn tin <3

\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 4X + 3O2 --to--> 2X2O3
2/15 <- 0,1 -------> 1/15
\(M_X=\dfrac{10,4}{\dfrac{2}{15}}=78\left(\dfrac{g}{mol}\right)\)
Bạn ơi đề có bị sai ko vậy :)?

\(CT:A_2O_n\)
\(\%A=\dfrac{2A}{2A+16n}\cdot100\%=70\%\)
\(\Leftrightarrow2A+16n=\dfrac{20}{7}A\)
\(\Leftrightarrow16n=\dfrac{6}{7}A\)
\(\Leftrightarrow A=\dfrac{56}{3}n\)
\(BL:n=3\Rightarrow A=56\)
\(CT:Fe_2O_3\)
\(n_{Fe_2O_3}=\dfrac{40}{160}=0.25\left(mol\right)\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(0.25...........0.75\)
\(m_{dd_{H_2SO_4}}=\dfrac{0.75\cdot98}{24.5\%}=300\left(g\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{300}{1.2}=250\left(ml\right)\)
Nhận thấy rằng oxit không phải trường hợp đặc biệt $Fe_3O_4$
Nên gọi CTTQ của oxit là $R_2O_x$
Ta có: \(\dfrac{2.R.100\%}{2R+16.x}=70\%\Rightarrow0,6R=11,2x\Rightarrow R=\dfrac{56}{3}x\)
Vậy oxit là $Fe_2O_3$
$Fe_2O_3+3H_2SO_4\rightarrow Fe_2(SO_4)_3+3H_2O$
Ta có: $n_{Fe_2O_3}=0,25(mol)\Rightarrow n_{H_2SO_4}=0,75(mol)\Rightarrow V=250(ml)$