Cho hỗn hợp gồm Mg và Fe có khối lượng 8,64 gam được chia thành hai phần bằng nhau.
Phần 1: Hòa tan hoàn toàn vào dung dịch HNO3 loãng, dư thoát ra 555ml hỗn hợp khí NO và NO2 đo ở 27,3° C và 2 atm và có tỉ khối hơi so với H2 bằng 18,8889.
Phần 2: Đem hòa tan vào 400ml dung dịch chứa AgNO3 và Cu(NO3)2. Sau phản ứng thu được chất rắn gồm 3 kim loại có khối lượng 7,68g. Hòa tan chất rắn này trong dung dịch HCl dư thấy khối lượng chất rắn đã giảm đi 21,88%. Nồng độ của dung dịch AgNO3 và Cu(NO3)2 trong dung dịch lần lượt là
A.0,15M và 0,1M
B. 0,1M và 0,1M
C.0,05M và 0,15M
D. 0,125M và 0,215M


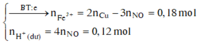
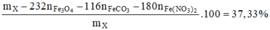
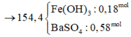

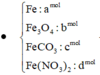
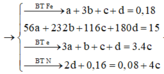
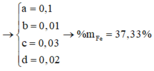

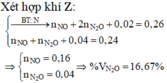


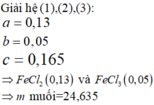



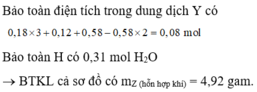


Đáp án C:
Gọi x, y là số mol Mg và Fe trong mỗi phần
=> 24x+56y = 4,32
Phần 2: Gọi a, b lần lượt là số mol của AgNO3 và Cu(NO3)2
Sau phản ứng có 3 kim loại là Ag, Cu và Fe dư.
Gọi số mol Fe tham gia phản ứng là t (mol)
Bảo toàn electron ta có: nenhường= ne nhận
Chỉ có duy nhất Fe dư tan trong HCl