Cho hơi nước đi qua than nóng đỏ, thu được 15,68 lít hỗn hợp khí X (đktc) gồm CO, CO2 và H2. Cho toàn bộ X tác dụng hết với CuO (dư) nung nóng, thu được hỗn hợp chất rắn Y. Hòa tan toàn bộ Y bằng dung dịch HNO3 (loãng, dư) được 8,96 lít NO (sản phẩm khử duy nhất, ở đktc). Phần trăm thể tích khí CO trong X là
A. 57,15%
B. 14,28%
C. 28,57%
D. 18,42%.


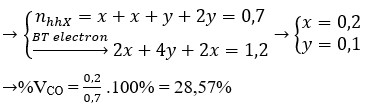
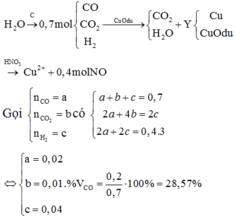
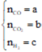 có
có 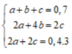
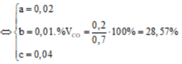
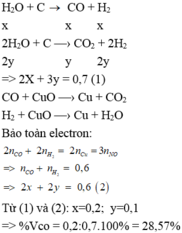

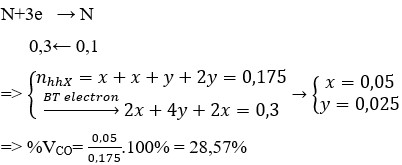
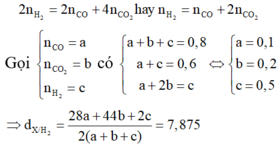
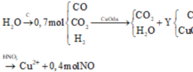
Quan sát – phân tích: Đề yêu cầu là tính phần trăm thể tích của CO. Vậy cái ta cần tìm chính là số mol của CO. Dựa vào sơ đồ ta nghĩ tới lập hệ phương trình 3 ẩn tương ứng với số mol của ba chất. Nhưng từ sơ đồ ta chỉ có thể lập được 2 hệ phương trình vậy thì không thể giải được bằng cách này. Vậy bài tập này sẽ có gì đó đặc biệt hoặc là phải biện luận. Khi viết phương trình phản ứng ra ta thấy:
Cả hai phương trình này đều tạo ra H2. Vậy chúng ta chỉ cần gọi 2 ẩn là có thể biểu diễn được số mol của H2 theo hai ẩn đó.
Kết hợp với dữ liệu còn lại ta tìm ngay được đáp án.
Gọi a và b lần lượt là số mol của CO và CO2 ⇒ Số mol của H2 là: n H 2 = a + 2 b
Theo giả thiết ta có: a + b +a + 2b = 0,7 ⇔ 2a + 3b = 0,7 (1)
Ta có: C u + 2 → C u 0 → C u + 2
Vậy ta sẽ bỏ qua bước trung gian là Cu và coi rằng (CO và H2) phản ứng với HNO3 tạo ra sản phẩm khử NO.
Áp dụng định luật bảo toàn electron ta có:
Đáp án C.