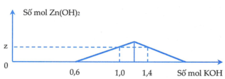
Khi nhỏ từ từ đến dư dung dịch KOH vào dung dịch hỗn hợp gồm x mol HCl và y mol ZnCl2, kết quả của thí nghiệm được biểu diễn trên đồ thị sau. Tổng (x + y + z) là
A. 0,9.
B. 2,0.
C. 1,1.
D. 0,8.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

KOH + HCl → KCl + H2O
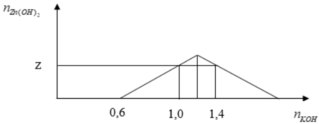
Khi nKOH = 0,6 thì bắt đầu xuất hiện kết tủa nHCl = x = 0,6
Khi nKOH = 1 thì Zn2+ vẫn còn dư
Zn2+ + 2OH- → Zn(OH)2
0,4 → 0,2
⇒ z = 0,2
Khi nKOH = 1,4 thì kết tủa đạt cực đại và bị tan bớt 1 phần
ZnCl2 + 2KOH → Zn(OH)2max + 2KCl
y → 2y → y
Zn(OH)2 + 2KOH → K2ZnO2 + 2H2O
y – 0,2 → 2y – 0,4
Ta có nKOH = 0,6 + 2y + 2y – 0,4 = 1,4 ⇒ y = 0,3
Vậy x + y + z = 0,6 + 0,3 + 0,2 = 1,1 ⇒ Chọn B.

Đáp án B
Tại 0,6 mol KOH thì bắt đầu có ⇒ axit vừa hết
⇒ x = 0 , 6 m o l
Mặt khác, tại 1 mol KOH thì chưa đạt cực đại
![]()
Xét tại 1,4 mol KOH: ta có công thức
![]()
![]()
![]()

Đáp án C
Từ đồ thị dễ dàng thấy được nNaOH = x = 0,6 mol.
Tại thời điểm nHCl = 0,8 mol ta thấy nAl(OH)3 = 0,2 mol.
Ta có nAlO2– chưa tạo kết tủa = 1 , 6 - 0 , 8 4 = 0 , 2
⇒ ∑nAlO2– = 0,2 + 0,2 = y = 0,4 mol.
⇒ nNaAlO2 = 0,4 mol ⇒ x + y = 1 mol

Đáp án C
Từ đồ thị dễ dàng thấy được
nNaOH = x = 0,6 mol.
Tại thời điểm nHCl = 0,8 mol
Ta thấy nAl(OH)3 = 0,2 mol.
Ta có:
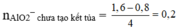
⇒ ∑nAlO2– = 0,2 + 0,2 = y = 0,4 mol.
⇒ nNaAlO2 = 0,4 mol
⇒ x + y = 1 mol
Chọn đáp án C
Nhìn vào đồ thị ta có n H C l = x = 0 , 6
Tại vị trí n K O H = 1 → z = 1 - 0 , 6 2 = 0 , 2
Tại vị trí n K O H = 1 , 4 = 0 , 6 + 2 y + 2 ( y - 0 , 2 ) → y = 0 , 3
=> x+y+z= 1,1
CHÚ Ý Các kim loại kiềm là: Li, Na, K, Rb, Cs. Các kim loại kiềm có nhiệt độ nóng chảy thấp hợp kim Na-K được dùng làm thiết bị báo cháy. Cs được dùng làm tế bào quang điện.