Điện phân( với điện cực trơ, có màng ngăn) dung dịch chứa m gam hỗn hợp gồm Cu(NO3)2 và NaCl bằng dòng điện có cường độ 2,68 A. Sau thời gian 6h, tại anot thoát ra 4,48 lít khí (đktc). Thêm 20,0 gam bột sắt vào dung dịch sau điện phân, thu được khí NO ( sản phẩm khử duy nhất của NO3‑) và 12, 4 gam chất rắn gồm hai kim loại. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 86,9.
B. 97,5.
C. 68,1
D. 77,5.



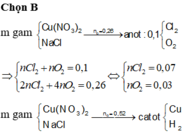





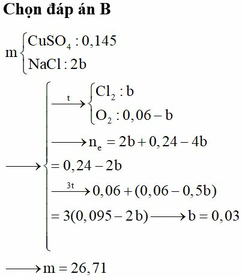
Đáp án A
I = 2,68 A; t = 6h ; nKhí = 4,48/22,4 = 0,2 (mol)
Tại catot xảy ra quá trình oxi hóa Cu2+ Tại anot xảy ra quá trình oxi hóa Cl-, H2O
Cu2+ +2e → Cu 2Cl- → Cl2 + 2e
a → 0,5a → 2a (mol)
2H2O → O2 + 4H+ + 4e
b → 0,5b → 2b → 2b (mol)
Vì dung dịch sau phản ứng tác dụng được với Fe và rắn thu được gồm 2 kim loại => Cu2+ còn dư sau quá trình điện phân. Và có khí NO thoát ra => tại anot H2O bị điện phân để sinh ra H+
=> nH+ = 2b = 0,4 (mol)
Vì Fe dư sau phản ứng nên Fe chỉ lên số oxi hóa +2; gọi số mol Cu2+ dư là x (mol)
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,15 ← 0,4 (mol)
Fe + Cu2+ → Fe2+ + Cu↓
x ← x → x (mol)
Khối lượng kim loại giảm: ∆ giảm = mFe phản ứng – mCu sinh ra
=> (20 – 12,4) = 0,15 + x).56 – 64x
=> x = 0,1 (mol)
=> nCu2+ bđ = nCu2+ đp + nCu2+ dư = 0,6/2 + 0,1 = 0,4 (mol)
=> m = mCu(NO3)2 + mNaCl = 0,4. 188 + 0,2. 58,5 = 86,9 (g)