Thực hiện phản ứng nhiệt phân nhôm hỗn hợp Al và Fe2O3 ( trong điều kiện không có không khí thu được 234,75 gam chất rắn X. Chia X thành hai phần:
Cho phần 1 tác dụng với dung dịch NaOH dư thu được 1,68 lít khí H2 ở đktc và m gam chất rắn. Hòa tan hết m gam chất rắn vào dung dịch H2SO4 đặc nóng thu được dung dịch chứa 82,8 gam muối và 0,6 mol SO2 là sản phẩm khử duy nhất.
Hòa tan hết phần 2 trong 12,97 lít dung dịch HNO3 1M, thu được hỗn hợp khí Y (gồm 1,25 mol NO và 1,51 mol NO2) và dung dịch A chứa các chất tan đều là muối, trong đó có a mol Fe(NO3)3. Biết các phản ứng hoàn toàn. Giá trị của a gần đúng với giá trị nào sau đây?
A. 1,10
B. 1,50
C. 1,00
D. 1,20.




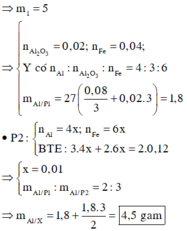


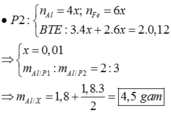
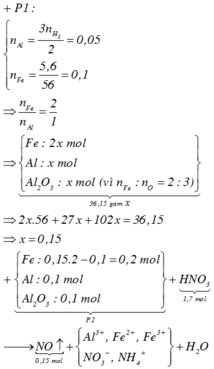
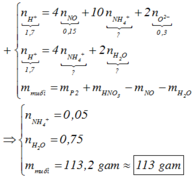
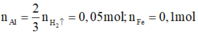
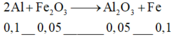
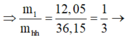
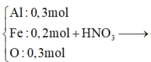
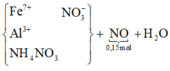
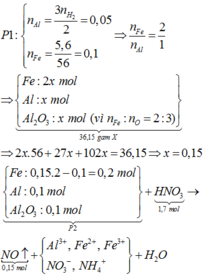
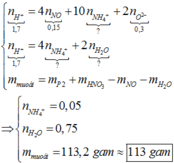
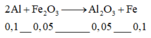
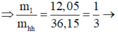
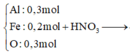
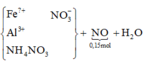
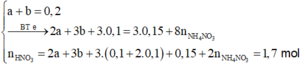
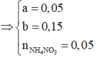
Giải thích:
Phần 1:
nH2 = 0,075 => nAldư = 0,05
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
8x→ 3x →4x → 9x
Chất rắn không tan trong NaOH là Fe (9x mol). Với H2SO4 đặc nóng
=> Fe3+ (u) và Fe2+ (v)
Bảo toàn electron: 3u + 2v = 0,6 . 2
m muối = 400a/2 + 152b = 82,8
=> u = 0,3 và v = 0,15
=> 9x = u + v => x = 0,05
Vậy phần 1 chứa Al (0,05), Al2O3 (0,2) và Fe (0,45)
=> mPhần 1 = 46,95
=> mPhần 2 = mX - mPhần 1 = 187,8
=> mPhần 2 = 4mPhần 1
Vậy phần 2 chứa các chất có số mol gấp 4 phần 1.
Phần 2 chứa Al (0,2), Al2O3 (0,8) và Fe (1,8)
=> nO = 0,8 . 3 = 2,4
nH+ = 12,97 = 4nNO + 2nNO2 + 2nO + 10nNH4+
=> nNH4+ = 0,015
Dung dịch A chứa Fe3+ (a mol), Fe2+ (y mol) và các ion khác.
Bảo toàn Fe => a + b = 1,8
Bảo toàn electron => 3a + 2b + 0,2 . 3 = 1,25 . 3 + 1,51 + 0,015 . 8
=> a = 1,18 và b = 0,62
Đáp án D