Cho một mẫu hợp kim Na-Ba tác dụng với nước (dư), thu được dung dịch X và 3,36 lít H2 (ở đktc). Thể tích dung dịch axit H2SO4 2M cần dùng để trung hoà dung dịch X là
A. 150 ml
B. 75 ml
C. 60 ml
D. 30 ml
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Na + H2O → NaOH + H2 (1)
Ba + 2H2O → Ba(OH)2 + H2 (2)
Theo (1) và (2) n OH - ( dd X ) = 2 n H 2 = 0 , 3 mol
Phương trình ion rút gọn của dung dịch axit với dung dịch bazơ là
H+ + OH- → H2O
⇒ n H + = n OH - = 0 , 3 mol → n H 2 SO 4 = 0 , 15 mol
⇒ V H 2 SO 4 = 0 , 15 2 = 0 , 075 lit
=> Đáp án B

Chọn A.
Hợp kim K - Ca tan trong nước tạo dung dịch kiềm, đặt hợp kim K - Ca là M:
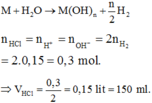

Đáp án C
M + nH2O → M(OH)n + n 2 H2.
Ta có: n H 2 = 0,035 mol → n O H - = 0,07 mol → n H + = 0,07 → V = 0,07 : 0,5 = 0,14 lít

Đáp án C
M + nH2O → M(OH)n + n/2 H2.
Ta có: n(H2) = 0,035 mol → n(OH-) = 0,07 mol
→ n(H+) = 0,07
→ V = 0,07 : 0,5 = 0,14 lít
Chọn B