Dung dịch axit sunfuric loãng có thể tác dụng với cả hai chất là
A. đồng và đồng(II) hiđroxit.
B. sắt và sắt(III) hiđroxit.
C. cacbon và cacbon đioxit.
D. Lưu huỳnh và hiđro sunfua
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Có 4 thí nghiệm tạo muối Fe2+ là (2), (4), (5) và (6)
Lưu ý ở thí nghiệm (1) Fe dư nhưng không phản ứng với FeCl3 vì đây không có môi trường điện li nên không phân li ra Fe3+ để phản ứng tạo Fe2+.

Đơn chất nào sau đây tác dụng với dung dịch axit sunfuric loãng sinh ra chất khí ?
A Lưu huỳnh
B Kẽm
C Bạc
D Cacbon
Pt : \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Chúc bạn học tốt

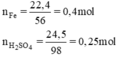
Phương trình hóa học của phản ứng:

So sánh tỉ lệ 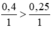 ⇒ Fe dư
⇒ Fe dư
Theo PT nFe (pư) = nH2SO4 = 0,25 mol ⇒ nFe dư = 0,4 – 0,25 = 0,15 mol
mFe dư = 0,15. 56 = 8,4g.
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4.
nH2 = nH2SO4 = 0,25 mol
Vkhí = 0,25 . 22,4 = 5,6l.

Chọn C
Vì A,C,D đều có p.ứng
A. CO2 + H2O \(⇌\) H2CO3
B. SO2 + H2O \(⇌\) H2SO3
D. N2O5 + H2O \(\rightarrow\) 2HNO3

a) nFe=0,4(mol); nH2SO4=0,5(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
Ta có: 0,4/1 < 0,5/1
=> Fe hết, H2SO4 dư. tính theo nFe.
=> nH2= nH2SO4(p.ứ)=nFe=0,4(mol)
=>nH2SO4(dư)=0,5-0,4=0,1(mol)
=>H2SO4(dư)=0,1.98=9,8(g)
b) V(H2,dktc)=0,4.22,4=8,96(l)
Đáp án B