Hòa tan hoàn toàn m gam Al trong dung dịch HNO3 loãng (dùng dư) thu được 3,36 lít khí NO (sản phẩm khử duy nhất của N+5; đo đktc). Giá trị của m là
A. 8,10.
B. 4,05.
C. 1,35.
D. 2,70.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
Al → Al+3 + 3e || N+5 + 3e → N+2
Bảo toàn electron: nAl = nNO = 0,15 mol
⇒ m = 4,05(g) ⇒ chọn B.

Giải thích:
Bảo toàn e : 3nAl = 3nNO
=> nAl = nNO = 0,15 mol => m = 4,05g
Đáp án B

Giải thích:
Bảo toàn e : 3nAl = 3nNO
=> nAl = nNO = 0,15 mol
=> mAl = 4,05g
Đáp án B

Chọn đáp án B
Phản ứng: Al + 4HNO3 → Al(NO3)3 + NO + 2H2O.
⇒ nAl = nNO = 3,36 ÷ 22,4 = 0,15 mol
⇒ m = mAl = 0,15 × 27 = 4,05 gam

Chọn đáp án B
Phản ứng: Al + 4HNO3 → Al(NO3)3 + NO + 2H2O.
⇒ nAl = nNO = 3,36 ÷ 22,4 = 0,15 mol
⇒ m = mAl = 0,15 × 27 = 4,05 gam → chọn đáp án B.

Chọn đáp án B
Bảo toàn e ta có 3nAl = 3nNO ⇒ nAl = nNO = 0,1 mol
⇒ VNO = 0,1 × 22,4 = 2,24 lít ⇒ Chọn B

Chọn đáp án B
Bảo toàn e ta có 3nAl = 3nNO ⇒ nAl = nNO = 0,1 mol
⇒ VNO = 0,1 × 22,4 = 2,24 lít ⇒ Chọn B

Đáp án B
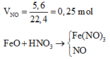
Quá trình cho nhận electron:
Fe+2 → Fe+3 + 1e N+5 + 3e → N+2
0,75 ← 0,75 0,75 ← 0,25
m F e O = 0,75.72 = 36 gam
Chọn đáp án B
Al → Al+3 + 3e || N+5 + 3e → N+2
Bảo toàn electron: nAl = nNO = 0,15 mol
⇒ m = 4,05(g) ⇒ chọn B.