Khi cho axit clohiđric tác dụng với kali pemanganat (rắn) để điều chế clo, khí clo sẽ thoát ra nhanh hơn khi
A. dùng axit clohiđric đặc và đun nhẹ hỗn hợp.
B. dùng axit clohiđric đặc và làm lạnh hỗn hợp.
C. dùng axit clohiđric loãng và đun nhẹ hỗn hợp.
D. dùng axit clohiđric loãng và làm lạnh hỗn hợp.

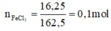
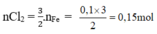
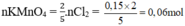
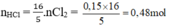
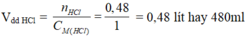
Chọn A
Dùng dung dịch HCl đặc và đun nhẹ hỗn hợp làm tăng tốc độ phản ứng