Trong tự nhiên Br có 2 đồng vị là 79Br, 81Br. Biết 79Br chiếm 54,5% số nguyên tử. Tìm khối lượng nguyên tử trung bình của Br.
A. 79,91.
B. 80,09.
C. 80,72.
D. 79,10.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nguyên tử khối của Brom là :
\(\overline{A}=\frac{79.50,69+81.49,31}{100}\approx79,98u\)
Vậy Nguyên tử khối trung bình của Brom là \(79,98u\)
Nguyên tử khối trung bình của Br là:
\(\overline{A}=\frac{79.50,69+81.49,31}{50,69+49,31}=\frac{7998,62}{100}=79,9862\)
Vậy nguyên tử khối trung bình của Br là 79,9862

Đáp án D
%41K = 100 - 93,26 - 0,012 = 6,728%.
Khối lượng nguyên tử trung bình của K là:
MK = 39 x 0,9326 + 40 x 0,00012 + 41 x 0,06728 = 39,13468.
Khối lượng nguyên tử trung bình của Br là:
MBr = 79,92.
Thành phần phần trăm của 39K trong KBr là
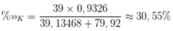

\(a.Đặt:\%^{79}Br=a\left(a>0\right)\\ \Rightarrow \%^{81}Br=100\%-a\\ \overline{NTK}_{Br}=79,91\\ \Leftrightarrow79a+81.\left(100\%-a\right)=79,91\\ \Leftrightarrow a=54,5\%\\ \Rightarrow\%^{79}Br=54,5\%;\%^{81}Br=45,5\%\)
b. Phần trăm theo KL đồng vị 79Br trong phân tử CaBr2:
\(54,5\%.\dfrac{70.91.2}{79,91.2+40}\approx43,59\%\)
c.
\(\left\{{}\begin{matrix}P=E\\P+N=79\\\left(P+E\right)-N=26\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P+N=79\\2P-N=26\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=35\\N=44\end{matrix}\right.\)

Ta có:
79,91=79.54,5%+A.(100-54,5)%
=>A=81
Đáp án A
Khối lượng nguyên tử trung bình của Br là
MBr = ( 79 . 54 , 5 + 81 ( 100 - 54 , 5 ) ) / 100 = 79 , 91