Ngâm một lá kim loại có khối lượng 50 gam trong dung dịch HCl. Sau khi thu được 336ml khí H2 (đktc) thì khối lượng lá kim loại giảm 1,68 %. Kim loại đó là :
A. Zn.
B. Fe.
C. Al.
D. Ni.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn Đáp án B
Gọi n là hóa trị của kim loại R cần tìm
Ta có : $n_{H_2} =\dfrac{336}{1000.22,4} = 0,015(mol) ; m_{R\ phản\ ứng} = 50.1,68\% = 0,84(gam)$
$2R + 2nHCl \to 2RCl_n + nH_2$
Theo PTHH :
$n_{H_2} = \dfrac{2}{n}n_{H_2} = \dfrac{0,03}{n}(mol)$
$\Rightarrow \dfrac{0,03}{n}.R = 0,84$
$\Rightarrow R = 28n$
Với n = 2 thì R = 56(Fe)$

Đáp án C
mKL giảm = 50.1,68% = 0,84g = mKL phản ứng
nH2 = 0,336: 22,4 = 0,015 mol
Gọi kim loại cần tìm là M có hóa trị n
M + nHCl → MCln + 0,5nH2
=> nM = 2/n.nH2 = 0,03/n mol
=> MM = 0,84: (0,03/n) = 28n
Với n = 2 => MM = 56 g/mol (Fe)

Em kiểm tra đề nha
Kim loại không giảm khối lượng đâu em
Đáp án B.
Khối lượng kim loại phản ứng là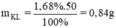
Số mol H2 là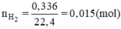
2M + 2n HCl → 2MCl2 + nH2
Số mol của M là:
→ {n = 2, M = 56} → M: Fe
Đặt kim loại cần tìm là X, có hóa trị n
Khối lượng kim loại giảm 1,68% → mX phản ứng = 50.1,68% = 0,84 gam
PTHH: 2X+ 2nHCl → 2XCln + nH2
Ta có: nX = (2/n).nH2 ⇔ (0,84/X) = (0,015.2/n)
⇔ X = 28n
Vậy X là Fe
B nha