Đốt cháy hoàn toàn 3 gam chất hữu cơ A chứa các nguyên tố C, H, O thu được 6,6 gam khí CO 2 và 3,6 gam H 2 O . Viết phương trình hoá học của phản ứng giữa A với Na.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi công thức của A là C x H y O z
Đốt cháy 3 gam A được 6,6 gam CO 2 và 3,6 gam H 2 O
Vậy m C trong 3 gam A là 6,6/44 x 12 = 1,8g
m H trong 3 gam A là 3,6/18 x 2 = 0,4g
Vậy trong 3 gam A có 3 - 1,8 - 0,4 = 0,8 (gam) oxi.
Ta có quan hệ:
60 gam A → 12x gam C → y gam H → 16z gam O
3 gam A → 1,8 gam C → 0,4 gam H → 0,8 gam O
=> x = 60 x 1,8 /36 = 3 ; y = 60 x 0,4/3 = 8
z = 60 x 0,8/48 = 1
Công thức của A là C 3 H 8 O

Bảo toàn C và H: \(n_C=n_{CO_2}=0,2(mol);n_H=2n_{H_2O}=0,6(mol)\)
Do đó \(m_O=4,6-0,2.12-0,6.1=1,6(g)\Rightarrow n_O=0,1(mol)\)
Đặt \(CTPT_Z:C_xH_yO_z\)
\(\Rightarrow x:y:z=0,2:0,6:0,1=2:6:1\\ \Rightarrow CTPT_Z:C_2H_6O\)

\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,4 (mol) => mC = 0,4.12 = 4,8(g)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
Bảo toàn H: nH = 0,9 (mol) => mH = 0,9.1 = 0,9 (g)
\(n_{N_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Bảo toàn N: nN = 0,1 (mol) => mN = 0,1.14 = 1,4 (g)

Chọn B.
Đốt cháy E thu được H2O (0,7 mol) và Na2CO3 (0,3 mol)
Muối thu được là RCOONa (0,2 mol) và R’(COONa)2 (0,2 mol)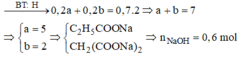
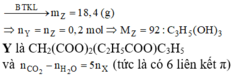
Vậy X là CH2(COO)2(CH≡C-COO)C3H5 Þ 8 nguyên tử H
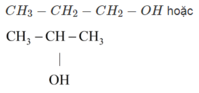

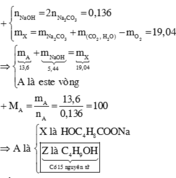
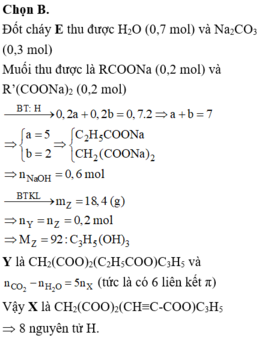
Phương trình hoá học của phản ứng giữa A với Na :