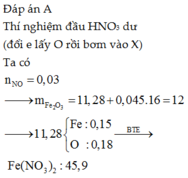
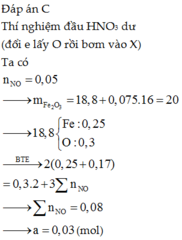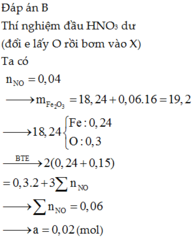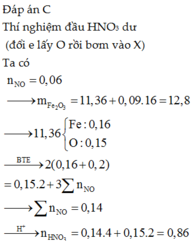Cho 18,8 gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư thu được 1,12lít khí NO sản phẩm khử duy nhất (ở đktc) và dung dịch Y. Dung dịch Y có thể hoà tan được tối đa 10,88 gam Cu (thu được a mol khí NO và dung dịch Z). Giá trị của a là:
A. 0,01
B. 0,02
C. 0,03
D. 0,04