Cho 15,6 gam hỗn hợp X gồm Al và Al2O3 tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí H2 (đktc). Khối lượng của Al2O3 trong X là:
A. 2,7 gam.
B. 5,1 gam.
C. 5,4 gam.
D. 10,2 gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Khi hòa tan hỗn hợp vào dung dịch NaOH dư thì chỉ có Al và A12O3 bị hòa tan.
Khi đó 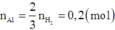
Khi hòa tan hỗn hợp vào dung dịch HCl (dư) thì cả ba chất trong hỗn hợp đều tan.
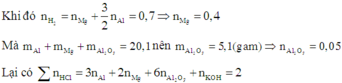
=> V = 2 (lít)

\(n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\)
Gọi \(\left\{{}\begin{matrix}n_{Al}=x\\n_{Mg}=y\end{matrix}\right.\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
x 3/2x
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}27x+24y=10,2\\\dfrac{3}{2}x+y=0,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Al}=0,2.27=5,4g\)
\(\Rightarrow m_{Mg}=0,2.24=4,8g\)
=> Chọn C

Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
a, Theo PT: \(n_{HCl}=3n_{Al}+6n_{Al_2O_3}=1,2\left(mol\right)\)
\(\Rightarrow m_{HCl}=1,2.36,5=43,8\left(g\right)\)
b, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
\(n_{AlCl_3}=n_{Al}+2n_{Al_2O_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{AlCl_3}=0,4.133,5=53,4\left(g\right)\)

Chọn B.
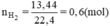
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↓
Al2O3 + 2NaOH → 2NaAlO2 + H2O
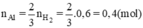
⇒ mAl = 27.0,4 = 10,8 (gam); mAl2O3 = 31,2 - 10,8 = 20,4 (gam).
Đáp án D