Hấp thụ hoàn toàn 6,6 gam CO2 bằng 200ml dung dịch NaOH 1M. Tính nồng độ mol của dung dịch thu được, coi thể tích dung dịch thay đổi ko đáng kể.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right);n_{NaOH}=0,2.1,75=0,35\left(mol\right)\)
Ta có: \(T=\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,35}{0,15}=\dfrac{7}{3}\approx2,33\) ⇒ pt tạo ra muối Na2CO3
PTHH: CO2 + 2NaOH → Na2CO3 + H2O
Mol: 0,15 0,3 0,15
\(C_{M_{ddNa_2CO_3}}=\dfrac{0,15}{0,2}=0,75M\)
\(C_{M_{ddNaOHdư}}=\dfrac{0,35-0,3}{0,2}=0,25M\)
PTHH: CO2 + NaOH ---> NaHCO3
Đổi 200ml = 0,2 lít
Ta có: \(V_{dd_{NaHCO_3}}=3,36+0,2=3,56\left(lít\right)\)
Ta có: \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{NaHCO_3}=n_{CO_2}=0,15\left(mol\right)\)
=> \(C_{M_{NaHCO_3}}=\dfrac{0,15}{3,56}=0,04M\)

\(n_{CO_2}=0,15mol\)
\(n_{NaOH}=0,35mol\)
\(T=\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,35}{0,15}=\dfrac{7}{3}>2\)\(\Rightarrow\) tạo muối \(Na_2CO_3\)
\(NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
0,35 0,15 0,15 0,15
\(\Rightarrow\)\(OH^-dư\) 0,2mol.
\(m_{ddsau}=0,35\cdot40+0,15\cdot44-0,15\cdot18=17,9g\)
\(C\%_{saup}\)\(_ư\)\(=\dfrac{15,9}{17,9}\cdot100=88,83\%\)

Đáp án A
nCO2=0,15 mol, nBa(OH)2=0,125 mol
1<nOH-/nCO2=0,25/0,15=1,67<2 => Tạo 2 muối
BaCO3: x
Ba(HCO3)2: y
x+y=nBa2+=0,125
x+2y=nC=0,15
=>x=0,1; y=0,025
CM Ba(HCO3)2=0,025/0,125=0,2M

$2K + 2H_2O \to 2KOH + H_2$
$n_{KOH} = n_K = \dfrac{21,06}{39} = 0,54(mol)$
Sau khi hòa tan :
$n_{KOH} = 0,54 + 0,4 = 0,94(mol)$
$C_{M_{KOH}} = \dfrac{0,94}{0,4} = 2,35M$

200ml = 0,2l
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,2 0,2
\(n_{FeCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(C_{M_{FeCl2}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Chúc bạn học tốt

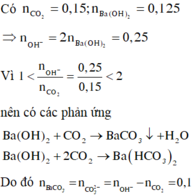
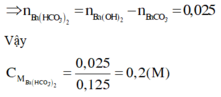

nCO2=6,6/44=0,15(mol)
nNaOH= 0,2.1= 0,2 (mol)
PTHH CO2 + 2NaOH--> Na2CO3 + H2O
0,1<-- 0,2----> 0,1
CO2 ( dư) + Na2CO3--> NaHCO3
0,05--> 0,05----> 0,05
CM Na2CO3= n/V= 0,1-0.05/0,2=0,25M
CM NaHCO3= n/V= 0.05/0,2=0,25M