Cho một hỗn hợp chứa 4,6g natri và 3,9g kali tác dụng với nước. Dung dịch sau phản ứng làm biến đổi màu giấy quỳ tím như thế nào?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,3 0,15
\(n_{Na}=\dfrac{6,9}{23}=0,3\left(mol\right)\)
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\)
0,1 0,05
\(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
\(V_{H_2}=0,05.22,4=1,12\left(l\right)\)
Dung dịch sau p/u biến đổi quỳ tím thành màu xanh vì dd có tính bazo

\(a,2Na+2H_2O\rightarrow2NaOH+H_2\\ 2K+2H_2O\rightarrow2KOH+H_2\\ b,n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right);n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\\ n_{H_2}=\dfrac{1}{2}.\left(0,2+0,1\right)=0,15\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=0,15.22,4=3,36\left(l\right)\\ c,Dung.dịch.sau.phản.ứng.có.KOH.và.NaOH.đều.là.kiềm.\\ \Rightarrow Quỳ.tím.hoá.xanh\)
\(n_{Na}=\dfrac{m}{M}=\dfrac{4,6}{23}=0,2mol\)
\(n_K=\dfrac{m}{M}=\dfrac{3,9}{39}=0,1mol\)
\(Na+2H_2O\rightarrow Na\left(OH\right)_2+H_2\)
\(K+2H_2O\rightarrow K\left(OH\right)_2+H_2\)
\(V_{H_2}=n_{H_2}.22,4=\left(0,2+0,1\right).22,4=6,72l\)
Dung dịch sau phản ứng làm quỳ tím chuyển sang màu xanh

a) 2Na+2H2O→2NaOH+H2(1)
2K+2H2O→2KOH+H2(2)
b) nNa=\(\dfrac{4,6}{23}\)=0,2(mol)
Theo PTHH (1): nNa:nH2=2:1
⇒nH2(1)=nNa.12=0,2.12=0,1(mol)
⇒VH2(1)=0,1.22,4=2,24(l)
nK=\(\dfrac{3,9}{39}\)=0,1(mol)
Theo PTHH (2): nK:nH2=2:1
⇒nH2(2)=nK.12=0,1.12=0,05(mol)
⇒VH2(2)=0,05.22,4=1,12(l)
⇒Vh2=2,24+1,12=3,36(l)
c) Dung dịch thu được sau phản ứng làm giấy quỳ tím chuyển đổi thành màu xanh vì nó là dung dịch bazơ.
d)
Fe2O3+3H2-to>2Fe+3H2O
0,15------0,1
n Fe2O3=0,1 mol
=>Fe2O3 dư
=>m Fe=0,1.56=5,6g

a) \(2Na+2H_2O\rightarrow2NaOH+H_2\left(1\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\left(2\right)\)
b) \(n_{Na}=\frac{4,6}{23}=0,2\left(mol\right)\)
Theo PTHH (1): \(n_{Na}:n_{H_2}=2:1\)
\(\Rightarrow n_{H_2\left(1\right)}=n_{Na}.\frac{1}{2}=0,2.\frac{1}{2}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2\left(1\right)}=0,1.22,4=2,24\left(l\right)\)
\(n_K=\frac{3,9}{39}=0,1\left(mol\right)\)
Theo PTHH (2): \(n_K:n_{H_2}=2:1\)
\(\Rightarrow n_{H_2\left(2\right)}=n_K.\frac{1}{2}=0,1.\frac{1}{2}=0,05\left(mol\right)\)
\(\Rightarrow V_{H_2\left(2\right)}=0,05.22,4=1,12\left(l\right)\)
\(\Rightarrow V_{h^2}=2,24+1,12=3,36\left(l\right)\)
c) Dung dịch thu được sau phản ứng làm giấy quỳ tím chuyển đổi thành màu xanh vì nó là dung dịch bazơ.

1)
a) Kim loại tan dần, chạy tròn trên mặt nước, xuất hiện khí không màu không mùi.
$2Na + 2H_2O \to 2NaOH + H_2$
$2K + 2H_2O \to 2KOH + H_2$
b) n Na = 4,6/23 = 0,2(mol) ; n K = 3,9/39 = 0,1(mol)
n H2 = 1/2 n Na + 1/2 n K = 0,15(mol)
V H2 = 0,15.22,4 = 3,36 lít
2)
a)
$Ba + 2H_2O \to Ba(OH)_2 + H_2$
$H_2 + CuO \xrightarrow{t^o} Cu + H_2O$
b) n H2 = n Ba = 6,85/137 = 0,05(mol)
V H2 = 0,05.22,4 = 1,12(lít)
c)
Ta thấy :
n CuO / 1 = 8/80 = 0,1(mol) < n H2 / 1 = 0,05 nên CuO dư
n CuO pư = n Cu = n H2 = 0,05(mol)
Suy ra :
m = m CuO dư + m Cu = (8 - 0,05.80) + 0,05.64 = 7,2(gam)

Ta có:
\(\left\{{}\begin{matrix}N_{Na}=\frac{4,6}{23}=0,2\left(mol\right)\\n_K=\frac{3,9}{39}=0,1\left(mol\right)\end{matrix}\right.\)
\(Na+H_2O\rightarrow NaOH+\frac{1}{2}H_2\)
0,2___0,2___0,2_______0,1__
\(K+H_2O\rightarrow KOH+\frac{1}{2}H_2\)
0,1__0,1____0,1____0,05_
\(\Rightarrow V_{H2}=\left(0,1+0,05\right).22,4=3,36\left(l\right)\)
Dd sau pứ là NaOH và KOH đều là dd bazo → Quỳ tím hóa xanh

Dung dịch sau phản ứng có chứa NaOH hay HNO 3 dư sẽ quyết định màu của quỳ tím.
- Số mol các chất đã dùng :
n NaOH = 10/40 mol; n HNO 3 = 10/63 mol
- Số mol NaOH nhiều hơn số mol HNO 3 . Theo phương trình hoá học, ta thấy khi phản ứng kết thúc, trong dung dịch còn dư NaOH. Do vậy, dung dịch sau phản ứng làm cho quỳ màu tím chuyển thành màu xanh.

a,\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right);n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,2 0,1
PTHH: 2K + 2H2O → 2KOH + H2
Mol: 0,1 0,05
b, \(n_{H_2}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
c,mdd sau pứ=4,6+3,9+91,5-0,15.2=99,7 (g)
\(\%m_{NaOH}=\dfrac{0,2.40.100\%}{99,7}=8,02\%\)
\(\%m_{KOH}=\dfrac{0,1.56.100\%}{99,7}=5,62\%\)
Bài 3 :
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
0,2 0,2 0,1
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
0,1 0,1 0,05
b) \(n_{H2\left(tổng\right)}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,15.22,4=3,36\left(l\right)\)
c) \(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(n_{KOH}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
⇒ \(m_{KOH}=0,1.56=5,6\left(g\right)\)
\(m_{ddspu}=8,5+91,5-\left(0,15.2\right)=99,7\left(g\right)\)
\(C_{NaOH}=\dfrac{8.100}{99,7}=8,02\)0/0
\(C_{KOH}=\dfrac{5,6.100}{99,7}=5,62\)0/0
Chúc bạn học tốt
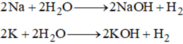
Dung dịch sau phản ứng làm biến đổi giấ quỳ hóa xanh vì sau phản ứng thu được dung dịch bazo ( NaOH, KOH).